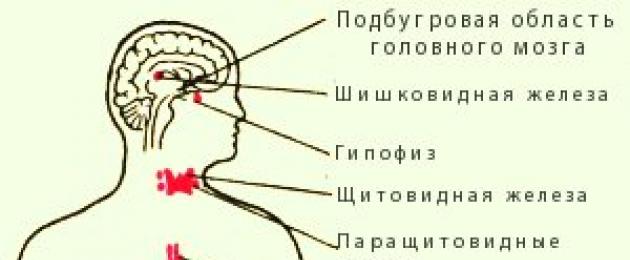
1. Физиологическая роль желез внутренней секреции. Характеристика действия гормонов.
Железы внутренней секреции — это специализированные органы, имеющие железистое строение и выделяющие свой секрет в кровь. У них отсутствуют выводные протоки. К таким железам относятся: гипофиз, щитовидная железа, околощитовидная железа, надпочечники, яичники, яички, зобная железа (тимус), поджелудочная железа, эпифиз, APUD - система(система захвата предшественников аминов и их декарбоксилирование), а также сердце - вырабатывает предсердный натрий-диуретический фактор, почки - вырабатывают эритропоэтин, ренин, кальцитриол, печень - вырабатывает соматомедин, кожа - вырабатывает кальциферол (витамин Д 3), ЖКТ - вырабатывает гастрин, секретин, холицистокинин, ВИП(вазоинтестинальный пептид), ЖИП(желудочноингибирующий пептид).
Гормоны выполняют следующие функции:
Участвуют в поддержание гомеостаза внутренней среды, контролируют уровень содержания глюкозы, объем внеклеточной жидкости, артериальное давление, баланс электролитов.
Обеспечивают физическое, половое, умственное развитие. А также отвечают за репродуктивный цикл (менструальный цикл, овуляция, сперматогенез, беременность, лактация).
Контролируют образование и использование питательных веществ и энергетически ресурсов в организме
Гормоны обеспечивают процессы адаптации физиологических систем к действию раздражителей внешней и внутренней среды и участвуют в поведенческих реакциях(потребность в воде, пище, половое поведение)
Являются посредниками в регуляции функций.
Железы внутренней секреции создают одну из двух систем регуляции функций. Гормоны отличаются от медиаторов, так как изменяют химические реакции в клетках на которые они действуют. Медиаторы вызывают электрическую реакцию.
Термин «гормон» происходит от греческого слова HORMAE - «возбуждаю, побуждаю».
Классификация гормонов.
По химическому строению :
1. Стероидные гормоны - производные холестерина (гормоны коры надпочечников, половых желез).
2. Полипептидные и белковые гормоны(передней доли гипофиза, инсулин).
3. Производные аминокислоты тирозина(адреналин, норадреналин, тироксин, трийодтиронин).
По функциональному значению:
1. Тропные гормоны (активируют деятельность других желез внутренней секреции; это гормоны передней доли гипофиза)
2. Эффекторные гормоны (действуют непосредственно на процессы обмена в клетках-мишенях)
3. Нейрогормоны (выделяются в гипоталамусе - либерины (активирующие) и статины (тормозящие)).
Свойства гормонов.
Дистантный характер действия (напр., гормоны гипофиза влияют на надпочечники),
Строгая специфичность гормонов(отсутствие гормонов приводит к выпадению определённой функции, и предупредить этот процесс можно только введением необходимого гормона),
Обладают высокой биологической активностью (образуются в малых концентрациях в ЖВС.),
Гормоны не обладают рядовой специфичностью,
Имеют короткий период полураспада (быстро разрушаются тканями, но имеют длительный гормональный эффект).
2. Механизмы гормональной регуляции физиологических функций. Ее особенности по сравнению с нервной регуляцией. Системы прямой и обратной (положительной и отрицательной) связей. Методы изучения эндокринной системы.
Внутренней секрецией (инкрецией) называется выделение специализированных биологически активных веществ - гормонов - во внутреннюю среду организма (кровь или лимфу). Термин "гормон" был впервые применен в отношении секретина (гормона 12-п.кишки) Старлингом и Бейлисом в 1902 году. Гормоны отличаются от других биологически активных веществ, например, метаболитов и медиаторов, тем, что они, во-первых, образуются высокоспециализированными инкреторными клетками, во-вторых, тем, что оказывают влияние через внутреннюю среду на отдаленные от железы ткани, т.е. обладают дистантным действием.
Наиболее древней формой регуляции является гуморально-метаболическая (диффузия активных веществ к соседним клеткам). Она в различной форме встречается у всех животных, особенно отчетливо проявляется в эмбриональном периоде. Нервная система по мере своего развития подчинила себе гуморально-метаболическую регуляцию.
Настоящие железы внутренней секреции появились поздно, но на ранних этапах эволюции есть нейросекреция . Нейросекреты - это не медиаторы. Медиаторы являются более простыми соединениями, работают локально в области синапса и быстро разрушаются, а нейросекреты - белковые вещества, расщепляются более медленно и работают на большом расстоянии.
С появлением кровеносной системы нейросекреты стали выделяться в ее полость. Затем возникли специальные образования для накопления и изменения этих секретов (у кольчатых), затем их вид усложнялся и эпителиальные клетки сами стали выделять свои секреты в кровь.
Эндокринные органы имеют самое разное происхождение. Часть из них возникли из органов чувств (эпифиз - из третьего глаза).Другие эндокринные железы образовалась из желез внешней секреции (щитовидная). Бранхиогенные железы образовались из остатков провизорных органов (тимус, паращитовидные железы). Стероидные железы произошли из мезодермы, из стенок целома. Половые гормоны выделяются стенками желез, содержащих половые клетки. таким образом, разные эндокринные органы имеют разное происхождение, но все они возникли как дополнительный способ регуляции. Есть единая нейрогуморальная регуляция, в которой ведущую роль играет нервная система.
Зачем образовалась такая добавка к нервной регуляции? Нервная связь - быстрая, точная, адресована локально. Гормоны - действуют шире, медленнее, дольше. Они обеспечивают длительную реакцию без участия нервной системы, без постоянной импульсации, что неэкономно. Гормоны имеют длительное последействие. Когда требуется быстрая реакция - работает нервная система. Когда требуется более медленная и стойкая реакция на медленные и длительные изменения среды - работают гормоны (весна, осень и т.п.), обеспечивая все адаптивные перестройки в организме, вплоть до полового поведения. У насекомых гормоны полностью обеспечивают весь метаморфоз.
Нервная система действует на железы по следующим путям:
1. Через нейросекреторные волокна вегетативной нервной системы;
2.Через нейросекреты - образование т.н. relising или inhibiting - факторов;
3. Нервная система может менять чувствительность тканей к гормонам.
Гормоны тоже влияют на нервную систему. Есть рецепторы реагирующие на АКТГ, на эстрогены (в матке), гормоны влияют на ВНД (половые), на активность ретикулярной формации и гипоталамуса и т.д. Гормоны оказывают влияние на поведение, мотивации и рефлексы, участвуют в стресс реакции.
Есть рефлексы, в которые в качестве звена включена гормональная часть. Например: холод -- рецептор -- ЦНС -- гипоталамус -- релизинг-фактор -- секреция тиреотропного гормона -- тироксин -- увеличение клеточного метаболизма -- повышение температуры тела.
Методы изучения желез внутренней секреции.
1.Удаление железы - экстирпация.
2. Трансплантация железы, введение вытяжки.
3. Химическая блокада функций железы.
4. Определение гормонов в жидких средах.
5. Метод радиоактивных изотопов.
3. Механизмы взаимодействия гормонов с клетками. Понятие о клетках-мишенях. Типы рецепции гормонов клетками мишенями. Понятие о мембранных и цитозольных рецепторах.
Пептидные (белковые) гормоны вырабатываются в форме прогормонов(их активация происходит при гидролитическом расщеплении), водорастворимые гормоны накапливаются в клетках в форме гранул, жирорастворимые (стероиды) - выделяются по мере образования.
Для гормонов в крови существуют белки-переносчики - это транспортные белки, способные связывать гормоны. При этом не происходит никаких химических реакций. Часть гормонов может переносится в растворенном виде. Гормоны доставляются ко всем тканям, но реагируют на действие гормонов только лишь клетки, обладающие рецепторами на действие гормона. Клетки, которые носят рецепторы называются клетки-мишени. Клетки-мишени подразделяются на: гормонзависимые и
гормончувствительные.
Различия между двумя этими группами состоит в том, что гормонзависимые клетки можут развиваться только в присутствии данного гормона. (Так, напр., половые клетки могут развиваться только при наличии половых гормонов), а гормончувствительные клетки могут развиваться без гормона, однако они способны воспринимать действие этих гормонов. (Так, напр., клетки нервной системы развиваются без воздействия половых гормонов, но воспринимают их действие).
Каждая клетка-мишень обладает наличием специфического рецептора к действию гормона, и часть рецепторов находится в мембране. Такой рецептор обладает стереоспецифичностью. У других клеток рецепторы расположены в цитоплазме - это цитозольные рецепторы, которые реагируют вместе с гормоном, проникающим внутрь клетки.
Следовательно, рецепторы делятся на мембранные и цитозольные. Для того, чтобы клетка отреагировала на действие гормона необходимо образование вторичных посредников к действию гормонов. Это характерно для гормонов с мембранным типом рецепции.
4. Системы вторичных посредников действия пептидных гормонов и катехоламинов.
Системами вторичных посредников действия гормонов являются:
1. Аденилатциклаза и циклический АМФ,
2. Гуанилатциклаза и циклический ГМФ,
3. Фосфолипаза С:
Диацилглицерол(ДАГ),
Инозитол-три-фсфат (ИФ3),
4. Ионизированный Ca - кальмодулин
Гетеротромный белок G-белок.
Этот белок образует в мембране петли и имеет 7 сегментов. Их сравнивают с серпантиновыми лентами. Имеет выступающую (наружную) и внутреннюю части. К наружной части присоединяется гормон,а на внутренней поверхности имеются 3 субъединицы - альфа, бета и гамма. В неактивном состоянии этот белок имеет гуанозиндифосфат. Но при активации гуанозиндифосфат меняется на гуанозинтрифосфат. Изменение активности G-белка приводит либо к изменению ионной проницаемости мембраны, либо в клетке активируется ферментная система (аденилатциклаза, гуанилатциклаза, фосфолипаза С). Это вызывает образование специфических белков, активируется протеинкиназа (необходима для процессов фосфолилирования).
G-белки могут быть активирующими (Gs) и ингибирующими, или по-другому, тормозящие(Gi).
Разрушение циклического АМФ происходит под действием фермента фосфодиэстеразы. Циклический ГМФ оказывает противоположное действие. При активации фосфолипазы C образуются вещества, которые способствуют накоплению внутри клетки ионизированного кальция. Кальций активирует протеинциназы, способствует мышечному сокращению. Диацилглицерол способствует превращению фосфолипидов мембраны в арахидоновую кислоту, которая является источником образования простагландинов и лейкотриенов.
Гормонрецепторный комплекс проникает в ядро и действует на ДНК, что меняет процессы транскрипции и образуется мРНК, которая выходит из ядра и идет к рибосомам.
Следовательно, гормоны могут оказывать:
1. Кинетическое или пусковое действие,
2. Метаболическое действие,
3.Морфогенетическое действие (дифференцировка тканей, рост, метаморфоз),
4. Корригирующие действие(исправляющие, приспосабливающее).
Механизмы действия гормонов в клетках:
Изменение проницаемости клеточных мембран,
Активация или угнетение ферментных систем,
Влияние на генетическую информацию.
Регуляция строится на тесном взаимодействии эндокринной и нервной системы. Процессы возбуждения в нервной системе могут активировать, либо тормозить деятельность эндокринных желез. (Рассмотрим, напр., процесс овуляции у кролика. Овуляция у кролика наступает только после акта спаривания, который стимулирует выделение гонадотропного гормона гипофиза. Последний вызывает процесс овуляции).
После перенесения психических травм может возникать тиреотоксикоз. Нервная система контролирует выделение гормонов гипофиза(нейрогормона), а гипофиз влияет на активность других желез.
Имеют место механизмы обратной связи. Накопление в организме гормона приводит к торможению выработки этого гормона соответствующей железой, а недостаток будет являться механизмом стимуляции образования гормона.
Существует механизм саморегуляции. (Напр., содержание глюкозы в крови определяет выработку инсулина и (или) глюкагона; если уровень сахара повышается вырабатывается инсулин, а если понижается — глюкагон. Недостаток Na стимулирует выработку альдостерона).
6. Аденогипофиз, связь его с гипоталамусом. Характер действия гормонов передней доли гипофиза. Гипо- и гиперсекреция гормонов аденогипофиза. Возрастные изменения образования гормонов передней доли.
Клетки аденогипофиза (их строение и состав смотрите в курсе гистологии) продуцируют следующие гормоны: соматотропин (гормон роста), пролактин, тиротропин (тиреотропный гормон), фолликулостимулирующий гормон, лютеинизирующий гормон, кортикотропин (АКТГ), меланотропин, бета-эндорфин, диабетогенный пептид, экзофтальмический фактор и гормон роста яичников. Рассмотрим более подробно эффекты некоторых из них.
Кортикотропин . (адренокортикотропный гормон - АКТГ) секретируется аденогипофизом непрерывно пульсирующими вспышками, имеющими четкую суточную ритмичность. Секреция кортикотропина регулируется прямыми и обратными связями. Прямая связь представлена пептидом гипоталамуса - кортиколиберином, усиливающим синтез и секрецию кортикотропина. Обратные связи запускаются содержанием в крови кортизола (гормон коры надпочечников) и за- мыкаются как на уровне гипоталамуса, так и аденогипофиза, причем прирост концентрации кортизола тормозит секрецию кортиколиберина и кортикотропина.
Кортикотропин обладает двумя типами действия - надпочечниковым и вненадпочечниковым. Надпочечниковое действие является основным и заключается в стимуляции секреции глюкокортикоидов, в существенно меньшей степени - минералокортикоидов и андрогенов. Гормон усиливает синтез гормонов в коре надпочечников - стероидогенез и синтез белка, приводя к гипертрофии и гиперплазии коры надпочечников. Вненадпочечниковое действие заключается в липолизе жировой ткани, повышении секреции инсулина, гипогликемии, повышенном отложении меланина с гиперпигментацией.
Избыток кортикотропина сопровождается развитием гиперкортицизма с преимущественным увеличением секреции кортизола и носит название "болезнь Иценко-Кушинга". Основные проявления типичны для избытка глюкокортикоидов: ожирение и другие метаболические сдвиги, падение эффективности механизмов иммунитета, развитие артериальной гипертензии и возможности возникновения диабета. Дефицит кортикотропина вызывает недостаточность глюкокортикоидной функции надпочечников с выраженными метаболическими сдвигами, а также падение устойчивости организма к неблагоприятным условиям среды.
Соматотропин . . Соматотропный гормон обладает широким спектром метаболических эффектов, обеспечивающих морфогенетическое действие. На белковый обмен гормон влияет, усиливая анаболические процессы. Он стимулирует поступление аминокислот в клетки, синтез белка за счет ускорения трансляции и активации синтеза РНК, увеличивает деление клеток и рост тканей, подавляет протеолитические ферменты. Стимулирует включение сульфата в хрящи, тимидина в ДНК, пролина в коллаген, уридина в РНК. Гормон вызывает положительный азотистый баланс. Стимулирует рост эпифизарных хрящей и их замену костной тканью, активируя щелочную фосфатазу.
Действие на углеводный обмен двояко. С одной стороны, соматотропин повышает продукцию инсулина как из-за прямого эффекта на бета клетки, так и из-за вызываемой гормоном гипергликемии, обусловленной распадом гликогена в печени и мышцах. Соматотропин активирует инсулиназу печени - фермент, разрушающий инсулин. С другой стороны, соматотропин оказывает контраинсулярное действие, угнетая утилизацию глюкозы в тканях. Указанное сочетание эффектов при наличии предрасположенности в условиях избыточной секреции может вызывать сахарный диабет, по происхождению называемый гипофизарным.
Действие на жировой обмен заключается в стимуляции липолиза жировой ткани и липолитического эффекта катехоламинов, повышении уровня свободных жирных кислот в крови; из-за избыточного поступления их в печень и окисления повышается образование кетоновых тел. Эти влияния соматотропина также относят к числу диабетогенных.
Если избыток гормона возникает в раннем возрасте, формируется гигантизм с пропорциональным развитием конечностей и туловища. Избыток гормона в юношеском и зрелом возрасте вызывает усиление роста эпифизарных участков костей скелета, зон с незавершенным окостенением, что получило название акромегалия. . Увеличиваются в размерах и внутренние органы - спланхомегалия.
При врожденном дефиците гормона формируется карликовость, получившая название "гипофизарный нанизм". Таких людей после выхода в свет романа Дж. Свифта о Гулливере называют в разговорной речи лилипутами. В других случаях приобретенный дефицит гормона вызывает не резко выраженное отставание в росте.
Пролактин . Секреция пролактина регулируется гипоталамическими пептидами - ингибитором пролактиностатином и стимулятором пролактолиберином. Продукция гипоталамических нейропептидов находится под дофаминэргическим контролем. На величину секреции пролактина влияет уровень в крови эстрогенов, глюкокортикоидов
и тиреоидных гормонов.
Пролактин специфически стимулирует развитие молочных желез и лактацию, но не его выделение, которое стимулируется окситоцином.
Помимо молочных желез, пролактин оказывает влияние на половые железы, способствуя поддержанию секреторной активности желтого тела и образованию прогестерона. Пролактин является регулятором водно-солевого обмена, уменьшая экскрецию воды и электролитов, потенцирует эффекты вазопрессина и альдостерона, стимулирует рост внутренних органов, эритропоэз, способствует проявлению инстинкта материнства. Помимо усиления синтеза белка, увеличивает образование жира из углеводов, способствуя послеродовому ожирению.
Меланотропин . . Образуется в клетках промежуточной доли гипофиза. Продукция меланотропина регулируется меланолиберином гипоталамуса. Основной эффект гормона заключается в действии на меланоциты кожи, где он вызывает депрессию пигмента в отростках, увеличение свободного пигмента в эпидермисе, окружающем меланоциты, повышение синтеза меланина. Увеличивает пигментацию кожи и волос.
7. Нейрогипофиз, связь его с гипоталамусом. Эффекты гормонов задней доли гипофиза (оксигоцина, АДГ). Роль АДГ в регуляции объема жидкости в организме. Несахарное мочеизнурение.
Вазопрессин . . Образуется в клетках супраоптического и паравентрикулярного ядер гипоталамуса и накапливается в нейрогипофизе. Основные стимулы, регулирующие синтез вазопрессина в гипоталамусе и его секрецию в кровь гипофизом в общем могут быть названы осмотическими. Они представлены: а) повышением осмотического давления плазмы крови и стимуляцией осморецепторов сосудов и нейронов-осморецепторов гипоталамуса; б) повышением в крови содержания натрия и стимуляцией гипоталамических нейронов, выполняющих роль рецепторов натрия; в) уменьшением центрального объема циркулирующей крови и артериального давления, воспринимаемыми волюморецепторами сердца и механорецепторами сосудов;
г) эмоционально-болевым стрессом и физической нагрузкой; д) активацией ренин- ангиотензиновой системы и стимулирующим нейросекреторные нейроны влиянием ангиотензина.
Эффекты вазопрессина реализуются за счет связывания гормона в тканях с двумя типами рецепторов. Связывание с рецепторами Y1-типа, преимущественно локализованными в стенке кровеносных сосудов, через вторичные посредники инозитолтрифосфат и кальций вызывает сосудистый спазм, что способствует названию гормона - "вазопрессин". Связывание с рецепторами Y2-типа в дистальных отделах нефрона через вторичный посредник ц-АМФ обеспечивает повышение проницаемости собирательных трубочек нефрона для воды, ее реабсорбцию и концентрацию мочи, что соответствует второму названию вазопрессина - "антидиуретический гормон, АДГ".
Кроме действия на почку и кровеносные сосуды, вазопрессин является одним из важных мозговых нейропептидов, участвующим в формировании жажды и питьевого поведения, механизмах памяти, регуляции секреции аденогипофизарных гормонов.
Недостаток или даже полное отсутствие секреции вазопрессина проявляется в виде резкого усиления диуреза с выделением большого количества гипотонической мочи. Этот синдром получил называние "несахарный диабет ", он бывает врожденным или приобретенным. Синдром избытка вазопрессина (синдром Пархона) проявляется
в чрезмерной задержке жидкости в организме.
Окситоцин . Синтез окситоцина в паравентрикулярных ядрах гипоталамуса и выделение его в кровь из нейрогипофиза стимулируется рефлекторным путем при раздражении рецепторов растяжения шейки матки и рецепторов молочных желез. Повышают секрецию окситоцина эстрогены.
Окситоцин вызывает следующие эффекты: а) стимулирует сокращение гладкой мускулатуры матки, способствуя родам; б) вызывает сокращение гладкомышечных клеток выводных протоков лактирующей молочной железы, обеспечивая выброс молока; в) оказывает при определенных условиях диуретическое и натриуретическое действие; г) участвует в организации питьевого и пищевого поведения; д) является дополнительным фактором регуляции секреции аденогипофизарных гормонов.
8. Кора надпочечников. Гормоны коры надпочечников и их функция. Регуляция секреции кортикостероидов. Гипо- и гиперфункция коры надпочечников.
Минералокортикоиды секретируются в клубочковой зоне коры надпочечников. Основным минералокортикоидом является альдостерон .. Этот гормон участвует в регуляции обмена солей и воды между внутренней и внешней средой, преимущественно воздействуя на канальцевый аппарат почек, а также потовые и слюнные железы, слизистую оболочку кишечника. Действуя на клеточные мембраны сосудистой сети и тканей, гормон обеспечивает также регуляцию обмена натрия, калия и воды между внеклеточной и внутриклеточной средой.
Основные эффекты альдостерона в почках - усиление реабсорбции натрия в дистальных отделах канальцев с его задержкой в организме и повышение экскреции калия с мочой с падением содержания катиона в организме. Под влиянием альдостерона происходит задержка в организме хлоридов, воды, усиленное выведение водородных ионов, аммония, кальция и магния. Увеличивается объем циркулирующей крови, формируется сдвиг кислотно-щелочного равновесия в сторону алкалоза. Альдостерон может оказывать глюкокортикоидное действие, однако оно в 3 раза слабее, чем у кортизола и в физиологических условиях не проявляется.
Минералокортикоиды являются жизненно важными гормонами, так как гибель организма после удаления надпочечников можно предотвратить, вводя гормоны извне. Минералокортикоиды усиливают воспаление, почему их называют иногда противовоспалительными гормонами.
Основным регулятором образования и секреции альдостерона является ангиотензин-II, что позволило считать альдостерон частью ренин-ангиотензин- альдостероновой системы (РААС), обеспечивающей регуляцию водно-солевого и гемодинамического гомеостаза. Звено обратной связи регуляции секреции альдостерона реализуется при изменении уровня калия и натрия в крови, а такжеобъема крови и внеклеточной жидкости, содержания натрия в моче дистальных канальцев.
Избыточная продукция альдостерона - альдостеронизм - может быть первичный и вторичный. При первичном альдостеронизме надпочечник из-за гиперплазии или опухоли клубочковой зоны (синдром Кона) продуцирует повышенные количества гормона, что ведет к задержке в организме натрия, воды, отекам и артериальной гипертензии, потере калия и водородных ионов через почки, алкалозу и сдвигам возбудимости миокарда и нервной системы. Вторичный альдостеронизм есть результат избыточного образования ангиотензина-II и повышенной стимуляции надпочечников.
Недостаток альдостерона при повреждении надпочечника патологическим процессом редко бывает изолированным, чаще сочетается с дефицитом и других гормонов коркового вещества. Ведущие нарушения отмечаются со стороны сердечно- сосудистой и нервной систем, что связано с угнетением возбудимости,
уменьшением ОЦК и сдвигами электролитного баланса.
Глюкокортикоиды (кортизол и кортикостерон ) оказывают влияние на все виды обмена.
На белковый обмен гормоны оказывают в основном катаболический и антианаболический эффекты, вызывают отрицательный азотистый баланс. распад белка происходит в мышечной, соединительной костной ткани, падет уровень альбумина в крови. Снижается проницаемость клеточных мембран для аминокислот.
Эффекты кортизола на жировой обмен обусловлены сочетанием прямых и опосредованных влияний. Синтез жира из углеводов самим кортизолом подавляется, но благодаря вызываемой глюкокортикоидами гипергликемии и повышению секреции инсулина происходит усиление образования жира. Жир откладывается в
верхней части туловища, на шее и на лице.
Эффекты на углеводный обмен в общем противоположны инсулину, почему глюкокортикоиды и называют контраинсулярными гормонами. Под влиянием кортизола возникает гипергликемия из-за: 1) усиленного образования углеводов из аминокислот путем глюконеогенеза; 2) подавления утилизации глюкозы тканями. Следствием гипергликемии являются глюкозурия и стимуляция секреции инсулина. Снижение чувствительности клеток к инсулину в совокупности с контраинсулярным и катаболическим эффектами может вести к развитию стероидного сахарного диабета.
Системные эффекты кортизола проявляются в виде снижения количества в крови лимфоцитов, эозинофилов и базофилов, увеличении нейтрофилов и эритроцитов, повышении сенсорной чувствительности и возбудимости нервной системы, увеличении чувствительности адренорецепторов к действию катехоламинов, поддержании оптимального функционального состояния и регуляции сердечно- сосудистой системы. Глюкокортикоиды повышают устойчивость организма к действию чрезмерных раздражителей и подавляют воспаление и аллергические реакции, почему из называют адаптивными и противовоспалительными гормонами.
Избыток глюкокортикоидов, не связанный с повышенной секрецией кортикотропина, получил название синдрома Иценко-Кушинга . Его основные проявления близки болезни Иценко-Кушинга, однако, благодаря обратной связи, секреция кортикотропина и его уровень в крови существенно снижены. Мышечная слабость, склонность к сахарному диабету, гипертензия и нарушения половой сферы, лимфопения, пептические язвы желудка, изменения психики - вот далеко не полный перечень симптомов гиперкортицизма.
Дефицит глюкокортикоидов вызывает гипогликемию, снижение сопротивляемости организма, нейтропению, эозинофилию и лимфоцитоз, нарушение адренореактив-ности и деятельности сердца, гипотензию.
9. Симпато-адреналовая система, ее функциональная организация. Катехоламины как медиаторы и гормоны. Участие в стрессе. Нервная регуляция хромаффинной ткани надпочечников.
Катехоламины - гормоны мозгового вещества надпочечников, представлены адреналином и норадреналином , которые секретируются в отношении 6:1.
Основными метаболическими эффектами. адреналина являются: усиление расщепления гликогена в печени и мышцах (гликогенолиз) за счет активации фосфорилазы, подавление синтеза гликогена, подавление потребления глюкозы тканями, гипергликемия, усиление потребления кислорода тканями и окислительных процессов в них, активация распада и мобилизация жира и его окисление.
Функциональные эффекты катехоламинов. зависят от преобладания в тканях одного из типов адренорецепторов (альфа или бета). Для адреналина основные функциональные эффекты проявляются в виде: учащения и усиления сердечных сокращений, улучшении проведения возбуждения в сердце, сужения сосудов кожи и органов брюшной полости; повышения теплообразования в тканях, ослабления сокращений желудка и кишечника, расслаблении бронхиальной мускулатуры, расширении зрачков, уменьшении клубочковой фильтрации и образования мочи, стимуляции секреции ренина почкой. Таким образом, адреналин вызывает улучшение взаимодействия организма с внешней средой, повышает работоспособность в чрезвычайных условиях. Адреналин является гормоном срочной (аварийной) адаптации.
Выделение катехоламинов регулируется нервной системой через симпатические волокна, проходящие в составе чревного нерва. Нервные центры, регулирующие секреторную функцию хромаффинной ткани, расположены в гипоталамусе.
10. Эндокринная функция поджелудочной железы. Механизмы действия ее гормонов на углеводный, жировой, белковый обмен. Регуляция содержания глюкозы в печени, мышечной ткани, нервных клетках. Сахарный диабет. Гиперинсулинемия.
Сахаро-регулирующими гормонами, т.е. влияющими на содержание сахара в крови и углеводный обмен, являются многие гормоны желез внутренней секреции. Но наиболее выраженные и мощные эффекты оказывают гормоны островков Лангерганса поджелудочной железы - инсулин и глюкагон . Первый из них может быть назван гипогликемическим, так как снижает уровень сахара в крови, а второй - гипергликемическим.
Инсулин оказывает мощное влияние на все виды обмена веществ. Действие его на углеводный обмен в основном проявляется следующими эффектами: он повышает проницаемость клеточных мембран в мышцах и жировой ткани для глюкозы, активирует и увеличивает содержание ферментов в клетках, усиливает утилизацию глюкозы клетками, активирует процессы фосфорилирования, подавляет распад и стимулирует синтеза гликогена, угнетает глюконеогенез, активирует гликолиз.
Основные эффекты инсулина на белковый обмен: повышение проницаемости мембран для аминокислот, усиление синтеза необходимых для образования белков
нуклеиновых кислот, прежде всего иРНК, активация в печени синтеза аминокислот, активация синтеза и подавление распада белков.
Основные эффекты инсулина на жировой обмен: стимуляция синтеза свободных жирных кислот из глюкозы, стимуляция синтеза триглицеридов, подавление распада жира, активация окисления кетоновых тел в печени.
Глюкагон вызывает следующие основные эффекты: активирует гликогенолиз в печени и мышцах, вызывает гипергликемию, активирует глюконеогенез, липолиз и подавление синтеза жира, повышает синтез кетоновых тел в печени, стимулирует катаболизм белков в печени, увеличивает синтез мочевины.
Основным регулятором секреции инсулина является D-глюкоза притекающей крови, активирующая в бета клетках специфический пул цАМФ и через этот посредник приводящая к стимуляции выброса инсулина из секреторных гранул. Усиливает ответ бета клеток на действие глюкозы гормон кишечника- желудочный ингибиторный пептид (ЖИП). Через неспецифический, независимый от глюкозы пул цАМФ стимулируют секрецию инсулина и ионы СА++. В регуляции секреции инсулина определенную роль играет и нервная система, в частности, блуждающий нерв и ацетилхолин стимулируют секрецию инсулина, а симпатические нервы и катехоламины через альфа-адренорецепторы подавляют секрецию инсулина и стимулируют секрецию глюкагона.
Специфическим ингибитором продукции инсулина является гормон дельта- клеток островков Лангерганса - соматостатин . Этот гормон образуется также и в кишечнике, где тормозит всасывание глюкозы и тем самым уменьшает ответную реакцию бета клеток на глюкозный стимул.
Секреция глюкагона стимулируется при снижении уровня глюкозы в крови, под влиянием гормонов ЖКТ (ЖИП, гастрин, секретин, панкреозимин- холецистокинин) и при уменьшении содержания ионов СА++, а угнетается - инсулином, соматостатином, глюкозой и кальцием.
Абсолютный или относительный по отношению к глюкагону недостаток инсулина проявляется в виде сахарного диабета.. При этом заболевании происходят глубокие расстройства обмена веществ и, если инсулиновую активность не восстанавливать искусственно извне, может наступить гибель. Для сахарного диабета характерны гипогликемия, глюкозурия, полиурия, жажда, постоянное чувство голода, кетонемия, ацидоз, слабость иммунитета, недостаточность кровообращения и многие другие нарушения. Крайне тяжелым проявлением сахарного диабета является диабетическая кома.
11. Щитовидная железа, физиологическая роль ее гормонов. Гипо- и гиперфункция.
Гормонами щитовидной железы являются трийодтиронин и тетрайодтиронин (тироксин ). Основным регулятором их выделения является гормон аденогипофиза тиротропин. Кроме того, существует прямая нервная регуляция щитовидной железы через симпатические нервы. Обратная связь осуществляется уровнем гормонов в крови и замыкается как в гипоталамусе, так и в гипофизе. Интенсивность секреции тиреоидных гормонов влияет на объем их синтеза в самой железе (местная обратная связь).
Основными метаболическими эффектами. тиреоидных гормонов являются: повышение поглощения кислорода клетками и митохондриями, активация окислительных процессов и повышение основного обмена, стимуляция синтеза белка за счет повышения проницаемости мембран клетки для аминокислот и активации генетического аппарата клетки, липолитический эффект, активация синтеза и экскреции холестерина с желчью, активация распада гликогена, гипергликемия, повышение потребления глюкозы тканями, повышение всасывания глюкозы в кишечнике, активация инсулиназы печени и ускорение инактивации инсулина, стимуляция секреции инсулина за счет гипергликемии.
Основными функциональными эффектами гормонов щитовидной железы являются: обеспечение нормальных процессов роста, развития и дифференцировки тканей и органов, активация симпатических эффектов за счет уменьшения распада медиатора, образования катехоламиноподобных метаболитов и повышения чувствительности адренорецепторов (тахикардия, потливость, спазм сосудов и др.), повышение теплообразования и температуры тела, активация ВНД и повышение возбудимости ЦНС, повышение энергетической эффективности митохондрий и сократимости миокарда, протекторный эффект по отношению к развитию повреждений миокарда и язвообразованию в желудке при стрессе, увеличение почечного кровотока, клубочковой фильтрации и диуреза, стимуляция процессов регенерации и заживления, обеспечение нормальной репродуктивной деятельности.
Повышенная секреция тиреоидных гормонов является проявлением гиперфункции щитовидной железы - гипертиреоза. При этом отмечаются характерные изменения обмена веществ (повышение основного обмена, гипергликемия, похудание и др.), симптомы избыточности симпатических эффектов (тахикардия, повышенная потливость, повышенная возбудимость, повышение АД и др.). Может
развиваться диабет.
Врожденная недостаточность тиреоидных гормонов нарушает рост, развитие и дифференцировку скелета, тканей и органов, в том числе и нервной системы (возникает умственная отсталость). Эта врожденная патология получила название "кретинизм". Приобретенная недостаточность щитовидной железы или гипотиреоз проявляются в замедлении окислительных процессов, снижении основного обмена, гипогликемии, перерождении подкожно-жировой клетчатки и кожи с накоплением глюкозаминогликанов и воды. Снижается возбудимость ЦНС, ослабляются симпатические эффекты и теплопродукция. Комплекс таких нарушений носит название "микседема", т.е. слизистый отек.
Кальцитонин - образуется в парафолликулярных К-клетках щитовидной железы. Органы-мишени для кальцитонина - кости, почки и кишечник. Кальцитонин снижает уровень кальция в крови, благодаря облегчению минерализации и подавлению резорбции костной ткани. Уменьшает реабсорбцию кальция и фосфата в почках. Кальцитонин тормозит секрецию гастрина в желудке и снижает кислотность желудочного сока. Секреция кальцитонина стимулируется повышением уровня Са++ в крови и гастрином.
12. Паращитовидные железы, их физиологическая роль. Механизмы поддержания
концентрации кальция и фосфатов в крови. Значение витамина Д.
Регуляция обмена кальция осуществляется в основном за счет действия паратирина и кальцитонина.Паратгормон, или паратирин, паратиреоидный гормон, синтезируется в околощитовидных железах. Он обеспе-чивает увеличение уровня кальция в крови. Органами-мишенями для этого гормона являются кости и почки. В костной ткани пара-тирин усиливает функцию остеокластов, что способствует демине-рализации кости и повышению уровня кальция и фосфора в плазме крови. В канальцевом аппарате почек паратирин стимулирует ре-абсорбцию кальция и тормозит реабсорбцию фосфатов, что приводит к гиперкальциемии и фосфатурии. Развитие фосфатурии может иметь определенное значение в реализации гиперкальциемического эффекта гормона. Это связано с тем, что кальций образует с фос-фатами нерастворимые соединения; следовательно, усиленное вы-ведение фосфатов с мочой способствует повышению уровня свобод-ного кальция в плазме крови. Паратирин усиливает синтез кальцитриола, который является активным метаболитом витамина D 3 . Последний вначале образуется в неактивном состоянии в коже под влиянием ультрафиолетового излучения, а затем под влиянием па-ратирина происходит его активация в печени и почках. Кальцитриол усиливает образование кальцийсвязывающего белка в стенке ки-шечника, что способствует обратному всасыванию кальция и раз-витию гиперкальциемии. Таким образом, увеличение реабсорбции кальция в кишечнике при гиперпродукции паратирина в основном обусловлено его стимулирующим действием на процессы активации витамина D 3 . Прямое влияние самого паратирина на кишечную стенку весьма незначительно.
При удалении околощитовидных желез животное погибает от тетанических судорог. Это связано с тем, что в случае низкого содержания кальция в крови резко усиливается нервно-мышечная возбудимость. При этом действие даже незначительных по силе внешних раздражителей приводит к сокращению мышц.
Гиперпродукция паратирина приводит к деминерализации и ре-зорбции костной ткани, развитию остеопороза. Резко увеличивается уровень кальция в плазме крови, в результате чего усиливается склонность к камнеобразованию в органах мочеполовой системы. Гиперкальциемия способствует развитию выраженных нарушений электрической стабильности сердца, а также образованию язв в пищеварительном тракте, возникновение которых обусловлено сти-мулирующим действием ионов Са 2+ на выработку гастрина и соляной кислоты в желудке.
Секреция паратирина и тиреокальцитонина (см. раздел 5.2.3) регулируется по типу отрицательной обратной связи в зависимости от уровня кальция в плазме крови. При снижении содержания кальция усиливается секреция паратирина и тормозится выработка тиреокальцитонина. В физиологических условиях это может наблю-даться при беременности, лактации, сниженном содержании кальция в принимаемой пище. Увеличение концентрации кальция в плазме крови, наоборот, способствует снижению секреции паратирина и увеличению выработки тиреокальцитонина. Последнее может иметь большое значение у детей и лиц молодого возраста, так как в этом возрасте осуществляется формирование костного скелета. Адекватное протекание этих процессов невозможно без тиреокальцитонина, оп-ределяющего абсорбцию кальция из плазмы крови и его включение в структуру костной ткани.
13. Половые железы. Функции женских половых гормонов. Менструально-овариальный цикл, его механизм. Оплодотворение, беременность, роды, лактация. Эндокринная регуляция этих процессов. Возрастные изменения выработки гормонов.
Мужские половые гормоны .
Мужские половые гормоны - андрогены - образуются в клетках Лейдига семенников из холестерола. Основным андрогеном человека является тестостерон . . Небольшие количества андрогенов образуются в коре надпочечников.
Тестостерон оказывает широкий спектр метаболических и физиологических эффектов: обеспечение процессов дифференцировки в эмбриогенезе и развития первичных и вторичных половых признаков, формирование структур ЦНС, обеспечивающих половое поведение и половые функции, генерализованное анаболическое действие, обеспечивающее рост скелета, мускулатуры, распределение подкожного жира, обеспечение сперматогенеза, задержку в организме азота, калия, фосфата, активацию синтеза РНК, стимуляцию эритропоэза.
Андрогены в небольших количествах образуются и в женском организме, являясь не только предшественниками синтеза эстрогенов, но и поддерживая половое влечение, а также стимулируя рост волос на лобке и в подмышечных впадинах.
Женские половые гормоны .
Секреция этих гормонов (эстрогенов ) тесно связана с женским половым циклом . Женский половой цикл обеспечивает четкую интеграцию во времени различных процессов, необходимых для осуществления репродуктивной функции - периодическую подготовку эндометрия к имплантации эмбриона, созревание яйцеклетки и овуляцию, изменение вторичных половых признаков и др. Координация этих процессов обеспечивается колебаниями секреции ряда гормонов, прежде всего гонадотропинов и половых стероидов. Секреция гонадотропинов осуществляется как "тонически", т.е. непрерывно, так и "циклически", с периодическим выбросом больших количеств фолликулина и лютеотропина в середине цикла.
Половой цикл длится 27-28 дней и делится на четыре периоды:
1) предовуляционный - период подготовки к беременности, матка в это время увеличивается в размерах, слизистая оболочка и ее железы разрастаются, усиливаются и учащается сокращение маточных труб и мышечного слоя матки, разрастается и слизистая оболочка влагалища;
2) овуляционный - начинается с разрыва пузырчатого яичникового фолликула, выхода из него яйцеклетки и продвижения ее по маточной трубе в полость матки. В этот период обычно наступает оплодотворение, половой цикл прерывается и наступает беременность;
3) послеовуляционный - у женщин в этот период появляется менструация, неоплодотворенная яйцеклетка, оставшаяся в матке несколько дней живой, погибает, нарастают тонические сокращения мускулатуры матки, приводящие к отторжению ее слизистой оболочки и выходу обрывков слизистой вместе с кровью.
4) период покоя - наступает после завершения послеовуляционного периода.
Гормональные сдвиги в течение полового цикла сопровождаются следующими перестройками. В предовуляционном периоде сначала происходит постепенно нарастание секреции фоллитропина аденогипофизом. Созревающий фолликул вырабатывает все большее количество эстрогенов, что по обратной связи начинает снижать продукцию фоллинотропина. Повышающийся уровень лютропина ведет к стимуляции синтеза ферментов, приводящих к истончению стенки фолликула, необходимой для овуляции.
В овуляционном периоде происходит резкий всплеск уровня в крови лютропина, фоллитропина и эстрогенов.
В начальной фазе постовуляционного периода происходит кратковременное падение и уровня гонадотропинов иэстрадиола , разорванный фолликул начинает заполняться лютеальными клетками, образуются новые кровеносные сосуды. Нарастает продукция прогестерона образующимся желтым телом, повышается секреция эстрадиола другими созревающими фолликулами. Создающийся уровень прогестерона и эстрогенов по обратной связи подавляет секрецию фоллотропина и лютеотропина. Начинается дегенерация желтого тела, падает в крови уровень прогестерона и эстрогенов. В секреторном эпителии без стероидной стимуляции возникают геморрагические и дегенеративные изменения, что приводит к кровотечению, отторжению слизистой, сокращению матки, т.е. к менструации.
14. Функции мужских половых гормонов. Регуляция их образования. Пре- и постнатальное влияние половых гормонов на организм. Возрастные изменения выработки гормонов.
Эндокринная функция семенников.
1) Клетки Сертолли - вырабатывают гормон-ингибин - тормозит образование фолллитропина в гипофизе, образование и секрецию эстрогенов.
2) Клетки Лейдига - вырабатывают гормон-тестостерон.
- Обеспечивает процессы дифференцировки в эмбриогенезе
- Развитие первичных и вторичных половых признаков
- Формирование структур ЦНС, обеспечивающих половое поведение и функции
- Анаболическое действие(рост скелета, мускулатуры, распределение подкожного жира)
- Регуляция сперматогенеза
- Задерживает в организме азот, калий, фосфат, кальций
- Активирует синтез РНК
- Стимулирует эритропоэз.
Эндокринная функция яичников.
В женском организме гормоны вырабатываются в яичниках и гормональной функцией обладают клетки гранулярного слоя фолликулов, которые вырабатывают эстрогены (эстрадиол, эстрон, эстриол) и клетки желтого тела (вырабатывают прогестерон).
Функции эстрогенов:
- Обеспечивают половую дифференцировку в эмбриогененезе.
- Половое созревание и развитие женских половых признаков
- Установление женского полового цикла, рост мышц матки, развитие молочных желез
- Определяют половое поведение, овогенез, оплодотворение и имплантацию в яйцеклетки
- Развитие и дифференцировку плода и течение родового акта
- Подавляют резорбцию кости, задерживают в организме азот, воду, соли
Функции Прогестерона:
1. Подавляет сокращение мускулатуры матки
2. Необходим для овуляции
3. Подавляет секрецию гонадотропина
4. Обладает антиальдостероновым действием, т. е. стимулирует натрийурез.
15. Зобная железа (тимус), ее физиологическая роль.
Вилочковую железу еще называют тимусом или зобной железой. Она, как и костный мозг, является центральным органом иммуногенеза (формирование иммунитета). Тимус распологается непосредственно за грудиной и состоит из двух долей (правой и левой), соединенных рыхлой клетчаткой. Тимус формируется раньше других органов иммунной системы, масса его у новорожденных 13 г., наибольшую массу - около 30 г - тимус имеет у детей 6-15 лет.
Затем он претерпевает обратное развитие (возрастная инволюция) и у взрослых почти полностью замещается жировой клетчаткой (у людей старше 50 лет жировая ткань составляет 90% от общей массы тимуса (в среднем 13-15 гр.)). С деятельностью тимуса связан период наиболее интенсивного роста организма. В тимусе находятся малые лимфоциты (тимоциты). Определяющая роль тимуса в формировании иммунной системы стала ясна из опытов, проведенных австралийским ученым Д. Миллером в 1961 г.
Он установил, что удаление тимуса у новорожденных мышей приводит к снижению выработки антител и увеличению продолжительности жизни пересаженной ткани. Эти факты указывали на то, что тимус принимает участие в двух формах иммунного ответа: в реакциях гуморального типа - выработке антител и в реакциях клеточного типа - отторжении (отмирании) пересаженной чужеродной ткани (трансплантата), которые происходят при участии разных классов лимфоцитов. За выработку антител ответственны так называемые В-лимфоциты, за реакции отторжения трансплантата - Т-лимфоциты. Т- и В-лимфоциты образуются путем различных превращений стволовых клеток костного мозга.
Проникая из него в тимус, стволовая клетка превращается под влиянием гормонов этого органа сначала в так называемый тимоцит, а затем, попадая в селезенку или лимфатические узлы, - в иммунологически активный Т-лимфоцит. Превращение стволовой клетки в В-лимфоцит происходит, по-видимому, в костном мозге. В вилочковой железе наряду с образованием из стволовых клеток костного мозга Т-лимфоцитов продуцируются гормональные факторы - тимозин и тимопоэтин.
Гормоны, обеспечивающие дифференцировку (различность) Т-лимфоцитов и играющие определенную роль в клеточных иммунных реакциях. Имеются также сведения, что гормоны обеспечивают синтез (построение) некоторых клеточных рецепторов.
Эндокринная система - система регуляции деятельности внутренних органов посредством гормонов, выделяемых эндокринными клетками непосредственно в кровь, либо диффундирующих через межклеточное пространство в соседние клетки.
Эндокринная система делится на гландулярную эндокринную систему (или гландулярный аппарат), в котором эндокринные клетки собраны вместе и формируют железу внутренней секреции, и диффузную эндокринную систему. Железа внутренней секреции производит гландулярные гормоны, к которым относятся все стероидные гормоны, гормоны щитовидной железы и многие пептидные гормоны. Диффузная эндокринная система представлена рассеянными по всему организму эндокринными клетками, продуцирующими гормоны, называемые агландулярными - (за исключением кальцитриола) пептиды. Практически в любой ткани организма имеются эндокринные клетки.
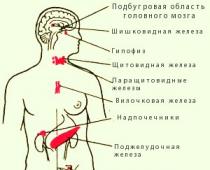
Эндокринная система. Главные железы внутренней секреции. (слева - мужчина, справа - женщина): 1. Эпифиз (относят к диффузной эндокринной системе) 2. Гипофиз 3. Щитовидная железа 4. Тимус 5. Надпочечник 6. Поджелудочная железа 7. Яичник 8. Яичко
Функции эндокринной системы
- Принимает участие в гуморальной (химической) регуляции функций организма и координирует деятельность всех органов и систем.
- Обеспечивает сохранение гомеостаза организма при меняющихся условиях внешней среды.
- Совместно с нервной и иммунной системами регулирует
- рост,
- развитие организма,
- его половую дифференцировку и репродуктивную функцию;
- принимает участие в процессах образования, использования и сохранения энергии.
- В совокупности с нервной системой гормоны принимают участие в обеспечении
- эмоциональных
- психической деятельности человека.
Гландулярная эндокринная система
Гландулярная эндокринная система представлена отдельными железами со сконцентрированными эндокринными клетками. Железы внутренней секреции (эндокринные железы) – органы, которые вырабатывают специфические вещества и выделяют их непосредственно в кровь или лимфу. Этими веществами являются гормоны – химические регуляторы, необходимые для жизни. Эндокринные железы могут быть как самостоятельными органами, так и производными эпителиальных (пограничных) тканей. К железам внутренней секреции относятся следующие железы:
Щитовидная железа
Щитовидная железа, вес которой колеблется от 20 до 30 г, расположена в передней части шеи и состоит из двух долей и перешейка – он расположен на уровне ΙΙ-ΙV хряща дыхательного горла и соединяет между собой обе доли. На задней поверхности двух долей парами расположены четыре околощитовидные железы. Снаружи щитовидная железа покрыта мышцами шеи, расположенными ниже подъязычной кости; своим фасциальным мешком железа прочно соединена с трахеей и гортанью, поэтому она перемещается вслед за движениями этих органов. Железа состоит из пузырьков овальной или округлой формы, которые заполнены белковым йодсодержащим веществом типа коллоида; между пузырьками располагается рыхлая соединительная ткань. Коллоид пузырьков вырабатывается эпителием и содержит гормоны, производимые щитовидной железой – тироксин (Т4) и трийодтиронин (Т3). Эти гормоны регулируют интенсивность обмена веществ, способствуют усвоению глюкозы клетками организма и оптимизируют расщепление жиров на кислоты и глицерин. Ещё один гормон, выделяемый щитовидной железой, – кальцитонин (по химической природе полипептид), он регулирует в организме содержание кальция и фосфатов. Действие этого гормона прямо противоположно паратиреоидину, который вырабатывается околощитовидной железой и повышает уровень кальция в крови, усиливает его приток из костей и кишечника. С этой точки действие паратиреоидина напоминает витамин D.
Паращитовидны железы
Паращитовидная железа регулирует уровень кальция в организме в узких рамках, так чтобы нервная и двигательная системы функционировали нормально. Когда уровень кальция в крови падает ниже определённого уровня, паращитовидной железы, чувствительные к кальцию, активируются и секретируют гормон в кровь. Паратгормон стимулирует остеокласты, чтобы те выделяли в кровь кальций из костной ткани.
Тимус
Тимус производит растворимые тимические (или тимусные) гормоны - тимопоэтины, регулирующие процессы роста, созревания и дифференцировки Т-клеток и функциональную активность зрелых клеток . С возрастом тимус деградирует, заменяясь соединительнотканным образованием.
Поджелудочная железа
Поджелудочная железа - крупный (длиной 12-30см) секреторный о́рган двойного действия (секретирует панкреатический сок в просвет двенадцатиперстной кишки игормоны непосредственно в кровоток), расположен в верхней части брюшной полости, между селезёнкой и двенадцатиперстной кишкой.
Инкреторный отдел поджелудочной железы представлен островками Лангерганса, расположенными в хвосте поджелудочной железы. У человека островки представленны различными типами клеток, вырабатывающими несколько полипептидных гормонов:
- альфа-клетки - секретируют глюкагон (регулятор углеводного обмена, прямой антагонист инсулина);
- бета-клетки - секретируют инсулин (регулятор углеводного обмена, снижает уровень глюкозы в крови);
- дельта-клетки - секретируют соматостатин (угнетает секрецию многих желез);
- PP-клетки - секретируют панкреатический полипептид (подавляет секрецию поджелудочной железы и стимулирует секрецию желудочного сока);
- Эпсилон-клетки - секретируют грелин («гормон голода» - возбуждает аппетит).
Надпочечники
На верхних полюсах обеих почек находятся небольшие железы треугольной формы – надпочечники. Они состоят из внешнего коркового слоя (80-90% массы всей железы) и внутреннего мозгового вещества, клетки которого лежат группами и оплетены широкими венозными синусами. Гормональная активность обеих частей надпочечников разная. Кора надпочечников вырабатывает минералокортикоиды и гликокортикоиды, имеющие стероидную структуру. Минералокортикоиды (важнейший из них – амид оох) регулируют ионный обмен в клетках и поддерживают их электролитическое равновесие; гликокортикоиды (например, кортизол) стимулируют распад белков и синтез углеводов. Мозговое вещество вырабатывает адреналин – гормон из группы катехоламина, который поддерживает тонус симпатической . Адреналин часто называют гормоном борьбы или бегства, так как его выделение резко возрастает лишь в минуты опасности. Повышение уровня адреналина в крови влечет за собой соответствующие физиологические изменения – учащается сердцебиение, сужаются кровеносные сосуды, напрягаются мышцы, расширяются зрачки. Ещё корковое вещество в небольших количествах вырабатывает мужские половые гормоны (андрогены). Если в организме возникают нарушения и андрогены начинают поступать в чрезвычайном количестве, у девочек усиливаются признаки противоположного пола. Кора и мозговое вещество надпочечников отличаются не только разных гормонов. Работа коры надпочечников активизируется центральной, а мозговое вещество – периферийной нервной системой.
ДАНИИЛ и половая активность человека были бы невозможными без работы гонад, или половых желёз, к которым относятся мужские яички и женские яичники. У маленьких детей половые гормоны вырабатываются в небольших количествах, но по мере взросления организма в определённый момент наступает быстрое увеличение уровня половых гормонов, и тогда мужские гормоны (андрогены) и женские гормоны (эстрогены) вызывают у человека появление вторичных половых признаков.
Гипоталамо-гипофизарная система
Железы внутренней секреции (эндокринные, инкреторные) - общее название желез, продуцирующих активные вещества (гормоны) и выделяющие их непосредственно во внутреннюю среду организма. Свое название железы внутренней секреции получили из-за неимения выводных протоков, поэтому образуемые ими гормоны выделяются непосредственно в кровь. К железам внутренней секреции относятся гипофиз, щитовидная железа, паращитовидные железы, надпочечники.
Кроме этого существуют железы, одновременно осуществляющие выделение веществ во внутреннуюю среду организма (кровь) и в полости организма (кишечник) или наружу, т.е. осуществляющие эндокринную и экзокринную функции. К таким железам, одновременно осуществляющим как внешнесекреторную, так и внутрисекреторную функции, относится поджелудочная железа (гормоны и поджелудочный сок, участвующий в пищеварении), половые железы (гормоны и репродуктивный материал - сперматозоид и яйцеклетка). Однако по установившейся традиции эти смешанные железы также относят к железам внутренней секреции, в совокупности объединенным в эндокринную систему организма. К железам смешанной секреции также относят вилочковую железу и плаценту, сочетающих выработку гормонов с неэндокринными функциями.

При помощи гормонов, вырабатываемых железами внутренней секреции, в организме осуществляется гуморальная (через жидкие среды организма - кровь, лимфу) регуляция физиологических функций, а так как все железы внутренней секреции иннервируются нервами и их деятельность находится под контролем центральной нервной системы, то гуморальная регуляция подчинена нервной регуляции, вместе с которой она составляет единую систему нейрогуморальной регуляции.
Гормоны - это высокоактивные вещества. Ничтожные их количества оказывают мощное воздействие на деятельность определенных органов и их систем. Особенность гормонов - специфическое влияние на строго определенный тип обменных процессов или на определенную группу клеток.
В ряде случаев одна и та же клетка может подвергаться действию многих гормонов, поэтому конечный биологический результат будет зависеть не от одного, а от многих гормональных влияний. С другой стороны гормоны могут влиять на какой-либо физиологический процесс прямо противоположно друг другу. Так, если инсулин снижает уровень сахара в крови, то адреналин повышает этот уровень. Биологические эффекты некоторых гормонов, в частности кортикостероидных, заключаются в том, что они создают условия для проявления действия другого гормона.
По химическому строению гормоны делятся на три большие группы:
- белки и пептиды - инсулин, гормоны передней доли гипофиза
- производные аминокислот - гормон щитовидной железы - тироксин и гормон мозгового вещества надпочечников - адреналин
- жироподобные вещества - стероиды - гормоны половых желез и коры надпочечников
Гормоны могут изменять интенсивность обмена веществ, влияют на рост и дифференцировку тканей, определяют наступление полового созревания. Влияние гормонов на клетки осуществляется разными путями. Некоторые из них действуют на клетки, связываясь с белками-рецепторами на их поверхности, другие проникают в клетку и активируют определенные гены. Синтез информационной РНК и следующий за этим синтез ферментов изменяют интенсивность или направленность обменных процессов.
Таким образом, эндокринная регуляция жизнедеятельности организма является комплексной и строго сбалансированной. Изменения физиологических и биохимических реакций под действием гормонов способствуют приспособлению организма к постоянно меняющимся условиям внешней среды.
Все железы внутренней секреции взаимосвязаны между собой: гормоны вырабатываемые одними железами, оказывают влияние на деятельность других желез, что обеспечивает единую систему координации между ними, которая осуществляется по принципу обратной связи [показать] .
Принцип обратной связи: усиленное выделение щитовидной железой тироксина тормозит выработку тиреотропного гормона гипофиза, который регулирует секрецию тироксина. Вследствие этого количество тироксина в крови падает. Уменьшение количества тироксина в крови ведет к прямо противоположному эффекту. Точно так же адренокортикотропный гормон гипофиза регулирует выработку гормонов корой надпочечников.
Главенствующая роль в этой системе принадлежит гипоталамусу, рилизинг-гормоны которого стимулируют деятельность главной железы внутренней секреции - гипофиза. Гормоны гипофиза в свою очередь регулируют деятельность других желез внутренней секреции.
Центральные регуляторные образования эндокринной системы
Гипоталамус - область промежуточного мозга, по своей анатомической сути не является железой внутренней секреции. Он представлен нервными клетками (нейронами) - гипоталамическими ядрами, которые синтезируют и секретируют гормоны непосредственно в кровеносное русло гипоталамо-гипофизарно-портальной системы.
Установлено, что гипоталамус является ведущим образованием в регуляции функции гипофиза при помощи гипофизотропных гормонов, получивших название рилизинг-гормоны. Рилизинг-гормоны синтезируются и секретируются нейронами гипоталамуса. Кроме этого установлено, что гормоны вазопрессин и окситоцин, ранее считавшиеся продуктами гипофиза, на самом деле синтезируются в нейронах гипоталамуса и секретируются ими в нейрогипофиз (задняя доля гипофиза), из которого они в дальнейшем секретируются в кровь в необходимые периоды жизни организма.
Существует представление о двойном механизме гипоталамической регуляции тропных функций гипофиза - стимулирующем и блокирующем. Однако до настоящего времени не удалось показать наличие нейрогормона, ингибирующего, например, секрецию гонадотропинов. Однако есть данные, свидетельствующие о ингибирующем действии мелатонина (гормона эпифиза), дофамина и серотонина на синтез в гипофизе гонадотропных гормонов ФСГ и ЛГ.
Яркой иллюстрацией двойного механизма гипоталамической регуляции тропных функций служит контроль секреции пролактина. Выделить и установить химическую структуру пролактин рилизинг-гормона не удалось. Основная роль в регуляции выделения пролактина принадлежит дофаминергическим структурам тубероинфундибулярной области гипоталамуса (туберогипофизарная дофаминовая система). Известно, что секрецию пролактина стимулирует тиролиберин, основная функция которого заключается в активации продукции тиреотропного гормона (ТТГ). Ингибитором секреции пролактина служит дофамин - катехоламин, предшественник синтеза адреналина и норадреналина.
Дофамин тормозит выделение пролактина из лактотрофов гипофиза. Антогонисты дофамина - резерпин, аминазин, метилдофа и другие вещества этой группы, истощают запасы дофамина в церебральных структурах, вызывают усиление выделения пролактина. Способность дофамина подавлять секрецию пролактина широко используется в клинике. Агонист дофамина бромкриптин (парлодел, карбеголин, достинекс) успешно применяется для лечения функциональной гиперпролактинемии и пролактинсекретирующей аденомы гипофиза.
Следует заметить, что дофамин не только регулирует секрецию пролактина, но и является одним из нейромедиаторов центральной нервной системы.
Эпифиз (шишковидное тело)
Шишковидное тело, или верхний мозговой придаток, у млекопитающих представляет собой паренхиматозный орган, исходящий из каудальной части крыши промежуточного мозга, не контактирующий с III желудочком, но соединенный с промежуточным мозгом ножкой, длина которой варьирует. У человека ножка тела эпифиза короткая, располагается непосредственно над крышей cреднего мозга.
Шишковидное тело включает три основных клеточных компонента: пинеалоциты, глию и нервные окончания, которые расположены преимущественно в околососудистом пространстве вблизи отростков пинеалоцитов.
Интенсивное изучение нервной регуляции функции шишковидного тела показало, что основными регуляторными стимулами являются свет и эндогенные механизмы генерации ритма . Световая информация передается в супрахиазматическое ядро по ретиногипоталамическому тракту. От супрахиазматического ядра идут аксоны к нейронам паравентрикулярного ядра, а от последнего - к верхней грудной интермедиолатеральной клеточной цепочке, которая иннервирует верхний шейный ганглий. Таков предположительный путь регуляции функций шишковидного тела. Считается, что ретиногипоталамический путь запускает механизм генерации ритма, который действует на остальной путь.
Мнения о роли шишковидного тела у человека противоречивы. Бесспорно лишь то, что оно не является рудиментарным органом, иногда дающим начало опухолям. Считается, что шишковидное тело проявляет метаболическую активность в течение большого периода жизни и секретирует мелатонин в соответствии с суточным ритмом; кроме того эпифиз выделяет и другие вещества, оказывающие антигонадотропное, антитиреоидное и антистероидное действие.
Мелатонин тормозит образование тиротропин-рилизинг-гормона, тиротропного гормона (ТТГ), гонадотропных гормонов (ЛГ, ФСГ), окситоцина, тиреоидных гормонов, тирокальцитонина, инсулина, а также синтез простагландинов; снижает сексуальную возбудимость и осветляет кожу путем воздействия на меланофоры.
Гипофиз, или нижний мозговой придаток, расположенный в средней части основания мозга, в углублении турецкого седла и соединяющийся ножкой с мозговым веществом (с гипоталамусом). Представляет собой железу массой 0,5 г. В нем выделяют два основных отдела: переднюю долю – аденогипофиз и заднюю – нейрогипофиз.

Аденогипофиз синтезирует и секретирует следующие гормоны:
- Гонадотропные гормоны - гонадотропины (гонады - половые железы, "тропос" - место)
- фолликулостимулирующий гормон (ФСГ)
- лютеинизирующий гормон (ЛГ)
Гонадотропины стимулируют деятельность мужских и женских половых желез и выработку ими гормонов.
- Адренокортикотропный гормон (АКТГ) - кортикотропин - регулирует деятельность коры надпочечников и выработку ею гормонов
- Тиреотропный гормон (ТТГ) - тиреотропин - регулирует функцию щитовидной железы и выработку ею гормонов
- Соматотропный гормон (СТГ) - соматотропин - стимулирует рост организма.
Избыточная продукция гормона роста у ребенка может привести к гигантизму: рост таких людей в 1,5 раза превышает рост нормального человека и может достичь 2,5 м. Если выработка гормона роста возрастает у взрослого человека, когда рост и формирование организма уже закончено, то развивается заболевание акрогемалия, при котором увеличиваются размеры рук, ног, лица. Одновременно растут и мягкие ткани: утолщаются губы и щеки, язык становится настолько большим, что не помещается во рту.
При его недостаточной выработке в раннем возрасте рост ребенка тормозится и развивается заболевание гипофизарная карликовость (рост взрослого человека не превышает 130 см). Гипофизарный карлик отличается от карлика-кретина (при заболевании щитовидной железы) правильными пропорциями тела и нормальным умственным развитием.
- Пролактин - регулятор фертильности и лактации у женщин
Нейрогипофиз накапливает синтезируемые в нервных ядрах гипоталамуса гормоны
- Вазопрессин - контролирует обратное всасывание воды в почечных канальцах на определенном уровне и является одним из факторов, определяющих постоянство водно-солевого обмена
в организме. Вазопрессин уменьшает мочевыделение, а также суживает кровеносные сосуды, что обусловливает повышение кровяного давления.
Понижение функции задней доли гипофиза вызывает несахарное мочеизнурение, при этом больной выделяет до 15 л мочи в сутки. Такая большая потеря воды требует ее восполнения, поэтому больные страдают от жажды и выпивают большое количество воды.
- Окситоцин - вызывает сокращение гладких мышц матки, кишечника, желчного и мочевого пузыря.
Периферические эндокринные железы
Щитовидная железа
Щитовидная железа располагается на передней стороне шеи, поверх щитовидного хряща. Ее масса составляет 16-23 г. Щитовидная железа продуцирует гормоны, в состав которых входит йод:
- Тироксин (Т 4) - основной гормон щитовидной железы - участвует в регуляции энергетического обмена, синтеза белка, роста и развития. Увеличение выделения этого гормона наблюдается
при базедовой болезни, когда повышается температура тела, человек худеет, несмотря на то что потребляет большое количество пищи. У него повышается артериальное давление, появляются
тахикардия (учащение частоты сердечных сокращений), мышечная дрожь, слабость, усиливается нервная возбудимость. Щитовидная железа при этом может увеличиваться в объеме и выступать
на шее в виде зоба.
При недостаточной деятельности щитовидной железы возникает микседема (слизистый отек) - заболевание, которое характеризуется понижением обмена веществ, падением температуры тела, замедлением пульса, вялостью движений. Масса тела увеличивается, кожа становится сухой, отечной. Причиной этого заболевания может быть или недостаточная активность самой железы, или недостаток в пище йода. В последнем случае йодная недостаточность компенсируется путем увеличения самой железы, вследствие чего развивается зоб.
Если недостаточность функции железы проявляется в детском возрасте, то развивается болезнь - кретинизм. Дети, страдающие этим заболеванием, слабоумны, у них задерживается физическое развитие.
Удаление щитовидной железы в молодом возрасте вызывает задержку роста млекопитающих. Животные остаются карликами, у них замедляется дифференцировка почти всех органов.
- Трийодтиронин (Т 3) - щитовидной железой секретируется не более 20%. Остальная часть Т 3 образуется путем дейодирования Т 4 вне щитовидной железы. Этот процесс обеспечивает почти 80% Т 3 образующегося за сутки. Внетиреоидное образование Т 3 из Т 4 происходит в тканях печени и почек.
- Кальцитонин (не содержит йод) - вырабатывается парафолликулярными клетками щитовидной железы. Органами-мишенями для кальцитонина является костная ткань (остеокласты) и почки (клетки восходящего колена петли Гентле и дистальных канальцев). Под влиянием кальцитонина тормозится активность остеокластов в кости, что сопровождается уменьшением резорбции костей и снижением содержания кальция и фосфора в крови. Кроме того, кальцитонин увеличивает экскрецию почками кальция, фосфатов, хлоридов.
Для нормальной работы щитовидной железы необходимо регулярное поступление йода в организм. В местностях, где почва и вода содержат мало йода, у людей и животных нередко наблюдается увеличение щитовидной железы - эндемический зоб. Этот зоб является компенсаторным приспособлением организма к недостатку иода. Благодаря увеличению объема железистой ткани щитовидная железа способна вырабатывать достаточное количество гормона, несмотря на пониженное поступление иода в организм. При этом она может увеличиваться до больших размеров и достигать массы 1 кг и более. Нередко обладатель такого зоба чувствует себя совершенно здоровым, так как эндемический зоб не сопровождается изменением функции щитовидной железы. В целях профилактики эндемического зоба в местностях, где мало йода в окружающей среде, к поваренной соли добавляется йодистый калий.
Паращитовидные железы
Паращитовидные (околощитовидные) железы (ОЩЖ) представляют собой округлой или овальной формы тельца, расположенные на задней поверхности долей щитовидной железы. Их количество непостоянно и может изменяться от 2 до 7-8. Нормальные паратироидные железы имеют размер 1 х 3 х 5 мм и весят от 35 до 40 мг. После 20-летнего возраста масса ОЩЖ не изменяется, у женщин она несколько больше, чем у мужчин.
ОЩЖ вырабатывают паратгормон, который регулирует обмен кальция и фосфора в организме. Этот гормон обусловливает всасывание кальция в кишечнике, высвобождение его из костей и обратное всасывание из первичной мочи в почечных канальцах.
Удаление или поражение паращитовидных желез ведет к спазмам мышц, судорогам, повышается возбудимость нервной системы. Такое состояние носит название тетании. Объясняется оно снижением концентрации кальция в крови. Возможна гибель от удушья вследствие судорог дыхательных мышц.
Вилочковая железа
Вилочковая железа, или тимус относится к числу смешанных желез. Ее внутрисекреторная функция заключается в выработке гормона - тимозина, модулирующего иммунные и ростовые процессы. Внешнесекреторная функция обеспечивает образование лимфоцитов, осуществляющих реакции клеточного иммунитета и регулирующих функции других лимфоцитов, вырабатывающих антитела.
Вилочковая железа располагается загрудинно, в верхнем отделе средостения.
Поджелудочная железа
Поджелудочная железа также относится к числу смешанных желез. Она расположена в брюшной полости, лежит на уровне тел 1-2 поясничных позвонков позади желудка, от которого отделяется сальниковой сумкой. Поджелудочная железа взрослого человека в среднем весит 80-100 г. Ее длина составляет 14-18 см, ширина - 3-9 см, толщина - 2-3 см. Железа имеет тонкую соединительнотканную капсулу и снаружи покрыта брюшиной. В железе выделяют головку, тело и хвост.
Внешнесекреторная функция поджелудочной железы заключается в секреции поджелудочного сока, который по выводным протокам попадает в двенадцатиперстную кишку и принимает участие в процессах расщепления питательных веществ.
Внутрисекреторную функцию выполняют особые клетки, расположенные островками (скоплениями), не связанными с выводными протоками. Эти клетки получили название панкреатических островков (островки Лангерганса). Величина островков составляет 0,1-0,3 мм, а общий вес - не превышает 1/100 массы железы. Больше всего островков расположено в хвосте поджелудочной железы. Островки пронизаны кровеносными капиллярами, эндотелий которых имеет фенестры, облегчающие поступление гормонов из островковых клеток в кровь через перикапиллярное пространство. В островковом эпителии выделяют 5 типов клеток:
- А-клетки (альфа-клетки, ацидофильные инсулоциты) - вырабатывают глюкагон при помощи которого происходит процесс превращения гликогена в глюкозу. Секреция этого гормона приводит к повышению уровня глюкозы в крови.
- В-клетки (бета-клетки) - секретируют инсулин, регулирующий уровень глюкозы в крови. Инсулин превращает избыток глюкозы в крови в животный крахмал гликоген и понижает уровень
сахара в крови. Под влиянием инсулина усиливается поглощение глюкозы периферическими тканями, а гликоген депонируется в печени и мышцах.
Удаление или поражение железы вызывает сахарный диабет. Недостаток или отсутствие инсулина приводит к резкому повышению сахара в крови и прекращению его превращения в гликоген. Избыток сахара в крови обусловливает его выделение с мочой. Расстройство углеводного обмена приводит к нарушению обмена белков и жиров, в крови накапливаются продукты неполного окисления жиров. При осложнениях заболевание может вызвать гипергликемическую (диабетическую) кому, при которой возникает расстройство дыхания, ослабление сердечной деятельности, потеря сознания. Первая помощь состоит в срочном введении инсулина.
Повышение секреции инсулина ведет к увеличению потребления глюкозы клетками тканей и отложению в печени и мышцах гликогена, снижению концентрации глюкозы в крови с развитием гипогликемической комы.
- Д-клетки (дельта-клетки) - вырабатывают соматостатин
- Д1-клетки (Д1-аргирофильные клетки) встречаются в островках в небольшом количестве, имеют в цитоплазме плотные гранулы, содержащие вазоактивный интестинальный полипептид
- РР-клетки - вырабатывают панкреатический полипептид
В клинической практике наибольшее значение гормоны, продуцируемые альфа и бета-клетками поджелудочной железы.
Надпочечники
Надпочечники представляют собой парный эндокринный орган, распологающийся в забрюшинном пространстве над верхними полюсами почек на уровне Тh XI - L I позвонков. Масса надпочечников взрослого человека в среднем составляет 5-8 г и, как правило, не зависит от пола и массы тела. Развитие и функцию коры надпочечников регулирует адренокортикотропный гормон гипофиза.
Надпочечники состоят из двух слоев, представленных соответственно корковым и мозговым веществом. В коре надпочечников выделяют клубочковую, пучковую и сетчатую зоны.
Надпочечники вырабатывают несколько гормонов:
- Гормоны мозгового слоя надпочечников - катехоламины: адреналин, норадреналин, дофамин, а также другие пептиды, в частности адреномедуллин.
Большое количество адреналина выделяется при сильных эмоциях - гневе, испуге, боли, напряженной мышечной или умственной работе. Увеличение количества поступающего в кровь адреналина вызывает учащенное сердцебиение, сужение кровеносных сосудов (однако сосуды мозга, сердца и почек расширяются) и повышение кровяного давления. Адреналин усиливает обмен веществ, особенно углеводов, ускоряет превращение гликогена печени и мышц в глюкозу. Под влиянием адреналина расслабляется мускулатура бронхов, угнетается перистальтика кишечника, повышается возбудимость рецепторов сетчатки, слухового и вестибулярного аппарата. Усиление образования адреналина может вызвать экстренную перестройку функций организма при действии чрезвычайных раздражителей.
Кроме того, катехоламины регулируют распад жиров (липолиз) и белков (протеолиз), когда источник энергии, мобилизованный из запасов углеводов, истощается. Под влиянием катехоламинов стимулируются процессы глкюконеогенеза в печени, где для образования глюкозы используют лактат, глицерин и аланин.
Наряду с непосредственным влиянием на обмен веществ катехоламины оказывают опосредованное действие через секрецию других гормонов (СТГ, инсулин, глюкагон, ренин-ангиотензиновая система и др.).
Адреномедуллин - принимает участие в регуляции гормонального, электролитного и водного баланса в организме, снижает артериальное давление, увеличивает частоту сердечных сокращений, расслабляет гладкую мускулатуру. Его содержание в плазме крови изменяется при различных патологических состояниях.
- Гормоны коркового слоя надпочечников
- гормоны клубочковой зоны - минералокортикоиды: альдостерон - регулирует солевой обмен (Nа + , К +) в организме. Избыток обусловливает повышение артериального давления (артериальную гипертензию) и снижение калия (гипокалиемию), недостаток - гиперкалиемию, которые могут оказаться несовместимыми с жизнью.
- гормоны пучковой зоны - глюкокортикоиды: кортикостерон, кортизол - регулируют углеводный и белковый обмен; угнетают выработку антител, обладают противовоспалительным действием, в связи с чем их синтетические производные широко применяются в медицине. Глюкокортикоиды поддерживают определенную концентрацию глюкозы в крови, увеличивают образование и отложение гликогена в печени и мышцах. Избыток или недостаток глюкокортикоидов сопровождается угрожающими жизни сдвигами.
- гормоны сетчатой зоны - половые гормоны: дегироэпиандростерон (ДГЭА), дегироэпиандростерон-сульфат (ДГЭА-с), андростендион, тестостерон, эстрадиол
При недостаточности функции коры надпочечников и снижении выработки гормонов развивается бронзовая, или аддисонова, болезнь. Ее характерные признаки - бронзовый оттенок кожи, мышечная слабость, повышенная утомляемость, восприимчивость к инфекции.
Половые железы
Половые железы - яичники у женщин и яички у мужчин - относятся к смешанным. Их внешнесекреторная функция заключается в образовании и выделении яйцеклеток и сперматозоидов, а внутрисекреторная - в продукции половых гормонов, поступающих в кровь.
Яичники - женские половые железы, представляют собой парный орган, выполняющий в организме генеративную и эндокринную функции. Располагается в полости малого таза, имеют овоидную форму, длина составляет 2,5-5,5 см, ширина - 2-2,5 см, масса - 5-8 г.
В яичниках образуются и созревают женские половые клетки (яйцеклетки), а также вырабатываются половые гормоны: эстрогены, прогестерон, андрогены , релаксин - размягчение шейки матки и лонного сочленения в период подготовки к родам, ингибин - тормозит секрецию ФСГ и некоторые другие полипептидные гормоны.
Яички - мужские половые железы - парный железистый орган, также выполняющий в организме генеративную и эндокринную функции. Располагается в мошонке, в области промежности. В яичках образуются и созревают мужские половые клетки (сперматозоиды), а также вырабатывается половой гормон - тестостерон и в незначительном количестве дигидроэпиандростерон и андростендион (большая часть их образуется в периферических тканях).
Половые гормоны - андрогены (у мужчин) и эстрогены (у женщин) стимулируют развитие органов размножения (половых желез и придаточных частей полового аппарата), созревание половых клеток и формирование вторичных половых признаков. Под вторичными половыми признаками подразумеваются те особенности в строении и функциях организма, которые отличают мужчин от женщин: строение скелета, развитие мускулатуры, распределение волосяного покрова, подкожного жира, строение гортани, тембр голоса, своеобразие психик» и поведения.
Действие половых гормонов на различные функции организма особенно наглядно проявляется у животных при удалении половых желез (кастрации) или их пересадке.
Большой интерес представляют опыты по пересадке половых желез: у ранее кастрированного животного появляются половые признаки того пола, железы которого пересажены. Например, если кастрированной курице пересадить половые железы петуха, то у нее появляются гребень, петушиное оперение и драчливость. Напротив, если кастрированному петуху пересадить яичник, то гребень уменьшается, исчезает петушиный задор. Такие "петухи" проявляют заботу о потомстве и высиживают цыплят.
Кастрация была распространена в России в некоторых религиозных сектах. В Италии до середины XIX в. практиковалась кастрация мальчиков, певших в церковном хоре, для сохранения у них высокого тембра голоса.
Регуляция деятельности желез внутренней секреции. Физиологические процессы в организме характеризуются ритмичностью , т. е. закономерной повторяемостью через определенные промежутки времени.
У млекопитающих и человека наблюдаются половые циклы, сезонные колебания физиологической активности щитовидной железы, надпочечников, половых желез, суточные изменения двигательной активности, температуры тела, частоты сердцебиения, обмена веществ и т. д.
Токсическое действие на железы внутренней секреции. Алкоголь и курение оказывают токсическое действие на железы внутренней секреции, в частности на половые железы, на генетический аппарат и развивающийся плод. У детей алкоголиков часто наблюдаются пороки развития, умственная отсталось, тяжелые заболевания.
Употребление спиртных напитков приводит к преждевременной старости, деградации личности, инвалидности и смерти. Великий русский писатель Л. Н. Толстой подчеркивал, что "вино губит телесное здоровье людей, губит умственные способности, губит благосостояние семьи и, что всего ужаснее, губит душу людей и их потомство".
Всесоюзное общество по распространению политических и научных знаний
Серия VIII выпуск I №18. Издательство «Знание» 1958. Тираж 55000 экз.
Введение
Болезни гипофиза
Надпочечники и их заболевания
Введение
Исторические сведения. Железы внутренней секреции человека. Гормоны и их роль в жизнедеятельности организма. Нервная система и эндокринные железы.
1 июня 1889 года на заседании Парижского биологического общества знаменитый ученый Броун-Секар выступил с сообщением, которое вызвало огромный интерес во всем мире. Броун-Секар, которому было в то время 72 года, заявил, что, впрыскивая себе под кожу вытяжки из половых желез (семенников) собак и морских свинок, он обнаружил исчезновение старческой дряхлости и поразительное увеличение физической силы и умственной работоспособности. Отметив омолаживающее действие экстрактов из мужских половых желез животных, французский ученый высказал предположение, что и другие железы, имеющиеся в организме человека и животных, выделяют в кровь какие-то вещества, без которых организм приходит в упадок и болезненное состояние.
Правда, и до Броун-Секара были известны отдельные факты, указывающие на большое значение для жизнедеятельности организма желез внутренней секреции, представлявшихся средневековым анатомам, описывавшим их при вскрытиях трупов людей и животных, загадочными образованиями.
Так, еще в глубокой древности было установлено, что удаление половых желез у самцов домашних животных (кастрация) вызывает и придает особо нежный вкус их мясу. На этом было основано повсеместно практиковавшееся холощение молодых петушков и боровков. Известно было также, что кастрация жеребцов и быков резко меняет их нрав и поведение, вследствие чего становится легче использовать их в упряжи. О влиянии, оказываемом кастрацией на голос человека, знали уже во времена Аристотеля.
Все эти сведения имели, однако, отрывочный характер и относились лишь к тем изменениям, которые наступают у животных и человека при удалении мужских половых желез.
В 1849 году немецкий ученый Бертгольд доказал, что если кастрировать петуха и затем пересадить ему удаленный семенник в любое другое место тела, то у такого петуха сохраняются яркий гребень и бородка, а также петушьи повадки — драчливость и способность петь, исчезающие у каплунов (кастратов). На основании этого первого научного эксперимента с эндокринной железой Бертгольд пришел к выводу, что вещество, выделяемое половыми железами, влияет через кровь на весь организм.
В 1855 году было открыто значение другой железы внутренней секреции - надпочечника. Английский врач Аддисон установил, что тяжелое разрушения надпочечников, чаще всего в результате поражения их туберкулезом. В том же 1855 году знаменитый французский физиолог Клод Бернар ввел в науку понятие о внутренней секреции, установив, что печень, кроме желчи, изливаемой в двенадцатиперстную кишку, вырабатывает и отдает непосредственно в кровь глюкозу. Тогда же он высказал предположение, что «органами, вырабатывающими внутренние секреты, являются селезенка, щитовидная железа, надпочечные железы и лимфатические железы».
В 1883 году швейцарские хирурги Кохер и Реверден описали болезненные явления, наступавшие после удаления щитовидной железы у человека. В 1886 году невропатологом Мари было описано новое заболевание - акромегалия, при которой у взрослого человека возобновляется рост костей; было установлено, что данная болезнь связана с нарушением деятельности небольшой железы внутренней секреции, расположенной у основания мозга, - гипофиза.
Почти ежегодно описывались новые, не известные ранее заболевания, связанные с нарушением функции желез внутренней секреции.
За последние 50 лет накоплено большое количество клинических и экспериментальных наблюдений в этой области. Значительный вклад внесли в эту отрасль знания отечественные ученые: В. Я. Данилевский, Л. В. Соболев, А. А. Богомолец, М. М. и Б. М. Завадовские, В. Д. Шервинский и другие. Учение о железах внутренней секреции выросло в самостоятельную науку - эндокринологию, установившую огромную роль этих желез в нормальном росте и развитии организма животного и человека. Большие успехи достигнуты также и в лечении эндокринных заболеваний, многие из которых еще недавно быстро приводили к гибели заболевших ими людей.
Теперь известно восемь желез внутренней секреции: гипофиз (мозговой придаток), эпифиз (шишковидная железа), щитовидная железа, зобная железа, околощитовидные железы (у человека их четыре), поджелудочная железа, надпочечники (два) и половые железы (две). Возможно, что в дальнейшем, по мере роста наших знаний, будут открыты новые, еще не изученные эндокринные органы.
В отличие от желез внешней секреции, например слюнных, потовых, сальных, почек, желез желудка и кишечника, которые выделяют продукты своей деятельности (слюну, пот, кожное сало, мочу, желудочный и кишечный сок) через выводные протоки наружу или в пищеварительный тракт, железы внутренней секреции не имеют выводных протоков. Вырабатываемые ими особые вещества - гормоны (от греческого слова «гормао», означающего «возбуждать», «приводить в действие») поступают прямо в кровь и разносятся ею по всем органам и тканям тела, усиливая и направляя в определенную сторону процессы жизнедеятельности организма.
Железы внутренней секреции находятся под контролем центральной и вегетативной нервной систем, которые регулируют интенсивность образования гормонов и скорость их поступления в кровь. В свою очередь гормоны влияют на деятельность нервной системы, тормозя или возбуждая активность клеток головного и спинного мозга.
Влияние нервной системы на железы внутренней секреции особенно отчетливо прослеживается при изучении эндокринных заболеваний, возникающих вслед за нервно-психическими потрясениями. Усиление же или ослабление работы желез внутренней секреции вызывает резкие изменения в психике и поведении человека и животных.
Щитовидная железа и ее заболевания
Микседема у детей и взрослых. Тиреотоксикозы (базедова болезнь). Лечение радиоактивным йодом. Простой зоб.
Щитовидная железа расположена на передней поверхности шеи, прикрывая лежащие под нею пищевод и трахею (дыхательное горло). Формой своей щитовидная железа, состоящая из двух боковых долей, соединенных между собой узким перешейком, напоминает бабочку с распростертыми крыльями. Длина долей щитовидной железы равна 5-8 см, ширина - 3-4 см и толщина 1,5-2,5 см. Вес этой железы у взрослого здорового человека обычно не превышает 25-30 г. Несмотря на это, щитовидная железа играет исключительно важную роль в жизнедеятельности организма.
Кровь поступает в развитую сеть кровеносных сосудов железы по четырем большим артериям; в течение одного часа вся кровь, циркулирующая в организме человека, успевает пройти через этот орган.
Если рассматривать щитовидную железу под микроскопом, то можно увидеть, что она состоит из большого количества пузырьков (фолликулов), внутри которых скапливается вязкое, полужидкое вещество (коллоид), вырабатываемое клетками железы (рис. 1). Каждый такой пузырек оплетен густой сетью мельчайших сосудов - капилляров, обильно снабжающих его кровью.
В коллоиде содержатся гормоны щитовидной железы - тироксин и трийодтиронин, образующиеся в результате соединения белка с йодом. Гормоны эти, доставляемые током крови во все ткани организма, принимают непосредственное участие в процессах тканевого обмена. Подсчитано, что в теле взрослого человека содержится всего 15 мг тироксина, но это ничтожное количество гормона необходимо для поддержания нормальной работы сердца, кишечника, почек, половых желез и многих других органов и систем.
Микседема. Если удалить щитовидную железу у молодого животного, например щенка, и прекратить таким образом поступление в кровь гормонов щитовидной железы, то рост животного приостанавливается. Веселый, жизнерадостный щенок становится вялым, целыми днями лежит неподвижно, температура тела у него понижается, кровяное давление падает ниже нормы; все процессы обмена замедляются. Щенок заметно отстает в росте и развитии. Такие же изменения наступают у ребенка, страдающего врожденным недоразвитием щитовидной железы или перенесшего какую-либо инфекцию, которая вызвала воспаление щитовидной железы, в результате чего уменьшилось или полностью прекратилось выделение в кровь соответствующих гормонов. Такой ребенок отстает в росте от сверстников и, если лечение не будет начато своевременно, остается на всю жизнь карликом (так называемый тиреогенный карликовый рост). Развитие таких детей также резко задерживается: ходить они начинают в 3-5 лет, а иногда и позже, зубы у них прорезаются очень поздно, не наступает вовремя смена молочных зубов; особенно страдает умственное развитие - первые слова они нередко произносят в возрасте 5-7 лет.
Характерен внешний вид детей, страдающих тяжелой формой недостаточности щитовидной железы - заболевания, называемого микседемой (в переводе это слово означает «слизистый отек»). Лицо у них одутловатое, выражение его тупое. Рот полуоткрыт, с толстым, высовывающимся из него языком. Голос из-за отека голосовых связок грубый, хриплый. Живот большой, часто с пупочной грыжей. Кожа по всему телу сухая, грубая. Волосы растут плохо (рис. 2).
| Рис. 2. Больная микседемой девушка 18 лет. Карликовый рост, вздутый живот с пупочной грыжей, отсутствие развития грудных желез. А и В — Врожденный гипотиреоз до и после лечения. | ||
 |
 |
|
Если микседема возникает у взрослого человека, то у него развиваются отеки всего тела, отличающиеся от отеков сердечного или почечного происхождения тем, что при надавливании пальцем на отечную кожу не остается ямки. Заболевшие микседемой жалуются на ухудшение памяти, апатию и вялость, общую слабость, сонливость, выпадение волос, ломкость ногтей. Им постоянно холодно (зябкость), температура тела понижена до 35-36°, даже инфекционные заболевания они переносят без значительного повышения температуры. В самое жаркое время года больные микседемой спят под теплым одеялом. Кожа у них становится сухой, шелушащейся (особенно на локтях и голенях); развиваются .
Достаточно больному микседемой начать принимать тиреоидин (имеющийся в аптеках препарат из высушенной щитовидной железы животных, изготовляемый на мясокомбинатах), как уже через короткий срок исчезают отеки, восстанавливается память, проходит сонливость, возвращаются энергия и жизнерадостность, прекращаются . Рост у детей, страдающих микседемой, после начала лечения тиреоидином возобновляется; понемногу исчезают и остальные признаки болезни. При правильном и систематическом лечении такие дети вырастают полноценными, здоровыми людьми.
Почти все больные микседемой - как дети, так и взрослые - должны принимать тиреоидин в течение всей жизни. Прекращение приема препарата влечет за собой возврат болезни. Только в редких случаях, если микседема возникла после операции на щитовидной железе, вследствие удаления почти всей ее ткани, могут наблюдаться случаи выздоровления от микседемы. Объясняется это тем, что оставшиеся после операции в небольшом количестве клетки щитовидной железы могут со временем разрастаться (регенерировать) и обеспечить потребность организма в гормонах щитовидной железы.
Тиреотоксикозы (базедова болезнь). Если при микседеме имеется недостаточное образование щитовидной железой гормонов, то при тиреотоксикозе, или базедовой болезни (по имени описавшего ее в 1840 году немецкого врача Карла Базедова), щитовидная железа, наоборот, вырабатывает чрезмерное количество тироксина и трийодтиронина.
В то время как микседема встречается относительно редко, тиреотоксикозы представляют собой одно из наиболее распространенных эндокринных заболеваний человека. Возникновение болезни, как это точно установлено, в огромном большинстве случаев (по наблюдениям профессора Н. А. Шерешевского у 80% больных) связано с какой-либо психической травмой или нервными переживаниями. На это указывал еще 70 лет назад выдающийся русский врач С. П. Боткин, который писал, что горе, испуг, гнев или страх могут быть причиной развития тяжелого тиреотоксикоза, возникающего иногда крайне быстро, в течение нескольких часов. Известны случаи, когда люди заболевали тиреотоксикозом тотчас же после пожара, железнодорожной или автомобильной катастрофы, вызвавших нервное потрясение, после тяжело переживаемой утраты близкого человека. Так, например, описано возникновение в течение одной ночи тяжелого тиреотоксикоза у женщины, потерявшей за несколько часов двух сыновей.
Каким же образом нервные переживания вызывают развитие этой болезни? Необычное возбуждение коры головного мозга, возникающее у человека при психическом потрясении, может передаваться щитовидной железе непосредственно по нервным путям или же идти по более сложному пути - через мозговой придаток (гипофиз), который, как установлено, выделяет особый тиреотропный гормон, усиливающий работу щитовидной железы. Образующиеся при этом в большом количестве гормоны щитовидной железы наводняют организм и вызывают его отравление. Поэтому болезнь и называют «тиреотоксикоз», что в переводе означает «отравление тироксином».
Женщины болеют тиреотоксикозом примерно в 8 раз чаще, чем мужчины. Наибольшее количество больных приходится на возраст от 20 до 40 лет, но могут заболеть и пожилые люди в возрасте 60-70 лет. Сравнительно редко заболевают тиреотоксикозом дети.
Внешний вид больных тиреотоксикозом, при ярко выраженной картине заболевания, очень характерен. Особенно обращает на себя внимание выпячивание глаз, придающее лицу больного гневное и несколько испуганное выражение (рис. 3). Признак выпячивания глаз (так называемый экзофтальм) наблюдается очень часто, но не является обязательным - встречаются больные, у которых этот признак отсутствует.
| Рис. 3. Слева - больная тиреотоксикозом, 42 лет. Резко выражен симптом пучеглазия, исчезнувший, как и все остальные признаки болезни, через 5 месяцев после лечения радиоактивным йодом (правый снимок). | ||
 |
 |
|
Больные тиреотоксикозом отличаются суетливостью, очень подвижны, вечно спешат, говорливы, легко возбудимы, раздражительны. Они сильно худеют, несмотря на то, что у многих имеется хороший или даже повышенный аппетит. Объясняется это тем, что у них значительно повышены процессы обмена и составные части пищи - белки, жиры и углеводы - сгорают гораздо быстрее, чем у здорового человека. Заболевшие тиреотоксикозом часто за несколько месяцев теряют в весе 12-16 кг и более и при длительном течении заболевания могут достигать крайних степеней истощения.
Постоянными признаками тиреотоксикоза являются увеличение щитовидной железы (зоб) и учащение сокращений сердца. Величина зоба не влияет существенно на тяжесть заболевания: иногда у серьезно больных зоб едва заметен и обнаруживается только при ощупывании шеи, в других же случаях при очень больших размерах зоба остальные признаки болезни выражены незначительно. По тяжести заболевания различают тяжелые формы тиреотоксикозов, случаи средней тяжести и легкие формы, не отражающиеся существенно на трудоспособности больных.
Сердцебиение у больных тяжелым тиреотоксикозом имеет постоянный характер и беспокоит больных и днем, и ночью. Вместо 72-80 ударов в минуту, являющихся нормой для здорового человека, число сердечных сокращений при тиреотоксикозе может достигать 120-160, а иногда и 200 в минуту. Такая непосильная работа быстро изнашивает сердечную мышцу, вызывает нарушения ритма, появление перебоев и, в конце концов, сердечную недостаточность (декомпенсацию) с отеками всего тела. Причиной смерти больных при тяжелых формах тиреотоксикоза чаще всего является недостаточность сердца. В конце прошлого столетия, когда не существовало еще надежных способов лечения этого заболевания, больные тяжелыми формами тиреотоксикоза погибали, по свидетельству С. П. Боткина, в течение 2-3 лет, а иногда и быстрее от сердечной недостаточности. В наше время такой исход болезни наблюдается редко и только в запущенных случаях, если лечение начато слишком поздно. Современная располагает радикальными средствами борьбы с этой болезнью.
До недавнего времени основным таким средством была операция удаления зоба. Поскольку конечной причиной болезни, как уже указывалось, является избыточное образование щитовидной железой гормонов и отравление ими организма, естественно было придти к мысли, что если хирургическим путем удалить большую часть щитовидной железы, то тем самым будет устранен источник поступления в кровь чрезмерного количества этих гормонов и больной должен выздороветь.
И, действительно, после такой операции от 80 до 90% больных тиреотоксикозом выздоравливает и восстанавливает свою трудоспособность. Однако оперативный способ лечения имеет и свои отрицательные стороны. Во время операции может быть случайно поврежден нижнегортанный нерв, в результате чего наступает временный или постоянный паралич голосовых связок и больной не в состоянии говорить полным голосом. Если вместе со щитовидной железой будут удалены и околощитовидные железы (небольшие образования величиной с мелкую горошину), то у оперированного развиваются приступы судорог (тетания), требующие постоянного лечения. Наконец, при значительном истощении больных и наличии у них признаков сердечной недостаточности подобная операция сопряжена с риском для жизни.
Правда, перечисленные выше осложнения наступают редко, но все же полностью гарантировать больного от них при оперативном методе лечения тиреотоксикозов невозможно.
Поэтому понятен тот большой интерес, который вызвал новый способ лечения тиреотоксикозов, не менее эффективный, чем оперативный метод, и в то же время совершенно безопасный для больных, а именно - лечение базедовой болезни радиоактивным йодом.
При этом способе лечения больным тиреотоксикозом дают выпить около четверти стакана бесцветного раствора, по внешнему виду ничем не отличимого от воды, содержащего некоторое количество радиоактивного йода. Спустя 2-3 недели больные начинают чувствовать улучшение, а через 2 месяца большинство из них полностью выздоравливает; лишь у части больных лечение приходится повторять.
В московской больнице имени С. П. Боткина в течение 1954-1957 годов нами было проведено лечение радиоактивным йодом свыше 1000 больных тяжелыми и средней тяжести формами тиреотоксикоза с неизменно хорошими результатами. Около 60% больных было излечено однократным приемом радиоактивного йода, у остальных лечение пришлось повторять 2-3 раза и очень редко - 4 или 5 раз. Даже в очень запущенных случаях, когда вследствие тяжести состояния вольных об оперативном вмешательстве не могло быть и речи, лечение радиоактивным йодом оказывалось успешным.
Каким же образом радиоактивный йод приводит к излечению такого тяжелого заболевания, как ярко выраженный тиреотоксикоз? Радиоактивный йод (J 131) принадлежит к числу искусственных радиоактивных изотопов, т. е. веществ, схожих по своим химическим свойствам с обычными распространенными в природе элементами, но отличающихся от них радиоактивностью - способностью излучать невидимые глазу лучи. Радиоактивный йод стал доступен для медицинских целей только в последние годы в связи с расширением использования атомной энергии в мирных целях. Так, в ядерном реакторе обыкновенный фосфор, атомный вес которого равен 31, может превратиться в радиоактивный с атомным весом 32, а обычный кобальт (Со 59) в радиоактивный кобальт с атомным весом 60. Радиоактивный йод с атомным весом 131 относится к числу так называемых «коротко живущих изотопов», так как период его полураспада равен всего восьми суткам, т. е. через восемь суток он теряет половину своей активности.
Будучи введен внутрь животному или человеку, радиоактивный йод быстро всасывается в желудочно-кишечном тракте и поступает в кровь, которая разносит его по всему организму. Щитовидная железа обладает «сродством» как к обычному, так и радиоактивному йоду и запасает его в больших количествах. Йод идет на построение вырабатываемых ею гормонов - тироксина и трийодтиронина (в состав молекулы первого входит четыре атома йода, в состав молекулы второго - три атома).
У здорового взрослого человека через 24 часа после того, как он получит радиоактивный йод, до 30% его оказывается захваченным щитовидной железой, остальные же 70% выводятся через почки с мочой.
У больных тиреотоксикозом способность железы к накоплению йода резко повышается и может достигать 70-90% введенной дозы. Иными словами, почти весь радиоактивный йод, введенный в организм больного тиреотоксикозом, оказывается захваченным щитовидной железой и в течение нескольких дней прочно удерживается ею.
Радиоактивный йод, распадаясь, испускает при этом гамма-лучи и бета-частицы. Гамма-лучи, легко проникающие через все ткани, не вызывают в железе никаких изменений. По-другому ведут себя бета-частицы. Они способны пробежать в тканях очень короткий путь - всего около 2 мм, а потому заканчивают свой пробег в самой толще щитовидной железы. Отдавая свою энергию клеткам железы, бета-частицы вызывают их гибель и прекращение выделения ими гормонов. Насколько сильна происходящая при этом бомбардировка клеток щитовидной железы бета-частицами, можно судить по тому, что в 1 милликюри радиоактивного йода каждую секунду образуется 37 миллионов бета-частиц (1 Кюри - единица измерения радиоактивности; милликюри - 1/1000 кюри). А ведь при лечении тиреотоксикозов мы в большинстве случаев вводим больным 6-8 милликюри радиоактивного йода.
Погибающие под действием бета-частиц клетки щитовидной железы съеживаются; на их месте образуется более плотная соединительная ткань. В результате происходит уменьшение или полное исчезновение зоба. Небольшое количество клеток, продолжающих вырабатывать умеренное количество гормонов, необходимых для жизнедеятельности организма, сохраняется лишь по периферии железы.
Таким образом, применением радиоактивного йода производится как бы бескровная операция. Функциональная активность железы значительно снижается, и больной тиреотоксикозом начинает выздоравливать. У большинства больных через 20 дней после приема радиоактивного йода постепенно исчезают сердцебиение, бессонница и дрожание рук, проходят часто сопутствующие тиреотоксикозу желудочно-кишечные расстройства, начинает увеличиваться вес тела (рис. 4). В последнюю очередь исчезает пучеглазие, которое иногда заметно еще многие месяцы, хотя все остальные признаки тиреотоксикоза уже прошли.
| Рис. 4. Слева - больная тиреотоксикозом, 46 лет. Справа - та же больная через 14 месяцев после начала лечения радиоактивным йодом; видно исчезновение зоба и пучеглазия; прибавила в весе на 7,5 кг. Полное выздоровление. | ||
 |
 |
|
Единственным осложнением, которого следует остерегаться при лечении тиреотоксикозов радиоактивным йодом, является наступление гипотиреоза, или микседемы (см. стр. 7). Это осложнение наблюдается в тех случаях, когда вследствие повышенной чувствительности щитовидной железы к действию радиоактивного йода наступает гибель всех клеток железы. Такая повышенная чувствительность наблюдалась нами у 5% больных, подвергавшихся лечению радиоактивным йодом; чтобы чувствовать себя вполне здоровым, им приходилось принимать 1-2 таблетки тиреоидина в день. После нескольких месяцев такого лечения микседема проходила.
Указанное осложнение при лечении радиоактивным йодом встречается не чаще, чем после оперативного лечения больных тиреотоксикозом. Вместе с тем терапия радиоактивным йодом обладает несомненными преимуществами перед хирургическим способом лечения тиреотоксикозов, так как избавляет больных от страха перед операцией и ее возможных осложнений.
Следует, однако, подчеркнуть, что не все случаи болезни подлежат лечению радиоактивным йодом. Быстрее всего поддаются излечению радиоактивным йодом больные, у которых заболевание вызвано диффузным (сплошным) увеличением щитовидной железы. При узловатом тиреотоксическом зобе и так называемой тиреотоксической аденоме предпочтительным способом лечения остается оперативный метод.
Простой зоб. Не всегда увеличение щитовидной железы сопровождается признаками, характерными для тиреотоксикоза. У человека может встречаться и так называемый простой зоб, при котором нет ни учащения пульса, ни пучеглазия, ни исхудания. Различают пять степеней зоба; при первой и второй степени увеличения щитовидной железы она не видна на глаз и определяется только при ощупывании шеи, при третьей степени - видно утолщение шеи и, наконец, при четвертой и пятой степени увеличения зоб достигает больших размеров и может затруднять дыхание и глотание (рис. 5).
| Рис. 4. Увеличение щитовидной железы (зоб) слева — 5-ой степени, справа 4-ой степени. | ||
 |
 |
 |
Причиной возникновения простого зоба в большинстве случаев является пониженная способность организма больного усваивать йод или недостаток йода в почве, воде и воздухе, а также в продуктах питания - овощах, молоке, мясе и др. Лечение простого зоба заключается в приеме больными в течение длительного срока лекарств, содержащих йод, под влиянием которого зоб постепенно уменьшается и может после нескольких лет лечения совсем исчезнуть.
В тех местностях, где часто встречается простой или, как его называют, эндемический (местный) зоб, производится йодирование соли, поступающей в продажу (на тонну соли прибавляют всего 10-25 г йодистого калия, так что эта добавка совершенно не ощутима на вкус при использовании йодированной соли в пищу). В СССР недостаток йода в природе отмечается в некоторых районах Урала, Кавказа, Алтая, Забайкалья, Марийской и Чувашской АССР, а также в отдельных пунктах Горьковской, Ивановской и Московской областей. В результате йодирования соли и других оздоровительных мероприятий, осуществленных при Советской власти, эндемический зоб, очень распространенный в прошлом среди населения этих мест, почти полностью ликвидирован.
Чтобы предупредить возможность развития зоба у детей, проживающих в таких местностях, им дают раз в неделю по таблетке «антиструмина» - препарата, содержащего йод, или 1-2 чайных ложки раствора йодистого калия.
Поджелудочная железа и ее заболевания
Сахарный диабет и современные методы его лечения. Применение инсулина и новых сульфаниламидных препаратов. Гипогликемическая болезнь.
Поджелудочная железа не только вырабатывает и выделяет в двенадцатиперстную кишку панкреатический сок, который содержит ферменты, расщепляющие белки, жиры и углеводы, но и отдает непосредственно в кровь гормон инсулин, без которого невозможно нормальное усвоение организмом сахара (глюкозы), являющегося основным источником питания всех тканей тела.
Одним из наиболее частых заболеваний, связанных с нарушением внутрисекреторной деятельности поджелудочной железы, является сахарное мочеизнурение, или сахарный . Количество больных диабетом весьма значительно. Так, в США, по последним статистическим данным, число страдающих сахарной болезнью превышает 2 миллиона человек. Сотни тысяч больных диабетом имеются и в других странах.
При возникновении диабета у человека появляются сильная жажда и учащенное мочеиспускание. Количество воды, чая и других жидкостей, которое выпивает больной диабетом, может достигать 6, 8 и даже 10 л в сутки вместо 1,5-2 л, потребляемых здоровым взрослым человеком. Соответственно возрастает и объем выводимой из организма мочи. Аппетит у больных диабетом нередко очень усиливается, однако, несмотря на это, больные теряют в весе по 3-5 кг и более за месяц и сильно худеют. При исследовании мочи больного в ней обнаруживается сахар, обычно отсутствующий в моче здорового человека. Потерей значительного количества сахара с мочой (до 300-500 г за сутки) и объясняется истощение и нарастающее исхудание больных диабетом.
Страдающие диабетом жалуются на общую слабость, боли в конечностях, ухудшение зрения и понижение работоспособности. Часто сопровождается различными кожными заболеваниями - экземой, появлением гнойничков и нарывов (фурункулов), а также зудом кожи, который не поддается никаким средствам, пока не будет установлена первопричина болезни и назначено правильное лечение. Очень часто при диабете наступают заболевания печени, почек и сердечно-сосудистой системы.
Появление сахара в моче является только одним из признаков диабета, представляющего собой хроническое расстройство многих видов обмена - в первую очередь углеводного, а затем жирового и белкового. В крови у больных диабетом содержится значительно больше сахара, чем у здоровых людей (обычно 200-300 и более мг% против 80-120 мг% у здоровых). Очень часто у больных диабетом повышается содержание в крови холестерина - одного из продуктов жирового обмена.
Диабетом болеют как мужчины, так и женщины. Начало заболевания приходится преимущественно на зрелый и пожилой возраст. Сравнительно редко заболевают дети и подростки, причем у них болезнь протекает обычно тяжелее, чем у взрослых. Причины, вызывающие сахарное мочеизнурение, разнообразны. Болезнь может возникнуть после различных инфекций, психических и физических травм, при чрезмерном питании, приведшем к ожирению, при воспалительных процессах и опухолях поджелудочной железы. Статистика указывает на роль наследственной предрасположенности к данному заболеванию: у 40% больных страдают диабетом также родители или ближайшие родственники. Иногда сочетается с другими эндокринными болезнями — акромегалией, гигантизмом, болезнью Иценко-Кушинга (см. заболевания гипофиза и надпочечников).
В большинстве случаев сахарного диабета непосредственной причиной, вызывающей нарушение углеводного, а вслед за ним жирового и белкового обмена, служит недостаточное образование в поджелудочной железе одного из ее гормонов - инсулина. Доказывается это следующим опытом. Если оперативным путем удалить у животного (собаки, кошки) всю поджелудочную железу, то у него всегда появляются признаки диабета - жажда, учащенное мочеиспускание, обнаруживается сахар в моче и повышается его содержание в крови. Достаточно, однако, начать вводить таким животным инсулин, как признаки диабета смягчаются и могут совсем исчезнуть, если инсулин вводить систематически и в достаточном количестве. При прекращении введения инсулина болезнь снова возвращается.
Помимо недостаточного образования инсулина, причиной диабета может быть повышенное выделение поджелудочной железой второго вырабатываемого ею гормона - глюкагона, обладающего прямо противоположным инсулину действием. Наконец, может быть следствием избыточного образования в печени особого фермента - инсулиназы, разрушающей инсулин.
Излечение диабета наблюдается чрезвычайно редко. В огромном большинстве случаев болезнь продолжается, в течение всей жизни. Поэтому правильный режим и соответствующее лечение являются необходимыми условиями сохранения трудоспособности и предотвращения осложнений, возникающих в запущенных случаях. Одним из наиболее опасных осложнений является диабетическая кома, которая может привести к смерти больного, если не будут приняты экстренные меры к его спасению.
Кома у больного диабетом представляет собой острое отравление организма недоокисленными продуктами жирового обмена - ацетоном, ацетоуксусной и бета-оксимасляной кислотами. Возникает кома в тех случаях, когда больной диабетом заболевает какой-либо инфекционной болезнью, при неправильном питании (излишнее употребление жирной пищи), употреблении спиртных напитков и при нерегулярном введении инсулина в тех случаях, когда нельзя обойтись без лечения этим гормоном. До открытия инсулина диабетическая кома в большинстве случаев заканчивалась смертью больного.
Инсулин был впервые получен в 1921 году в Канаде учеными Бантингом и Бестом и уже в 1922 году применен для лечения больных диабетом. Открытию инсулина предшествовало большое число экспериментальных исследований, произведенных на животных, причем особенно важное значение имели работы русского ученого Л. В. Соболева.
Открытие инсулина произвело переворот в лечении диабета и спасло жизнь сотням тысяч больных. В настоящее время лечение диабета заключается в установлении определенной индивидуальной диеты для каждого больного и систематическом введении инсулина. В легких случаях удается обходиться без инсулина и одной диетой добиваться удовлетворительного течения болезни.
Инсулин вводится больным диабетом под кожу с помощью шприца, так как принятый внутрь он разрушается пищеварительными соками и не оказывает никакого действия.
Однако при однократном подкожном введении инсулин действует короткий срок: через 6-8 часов содержание сахара в крови вновь начинает повышаться. Поэтому в тяжелых и средней тяжести случаях диабета приходится вводить инсулин 2-3 раза, а в редких случаях - даже 4 раза в день.
Известным шагом вперед в деле лечения больных диабетом является внедрение в медицинскую практику протамин-цинкинсулина, производство которого освоено в 1957 году московским заводом эндокринных препаратов. Это соединение, представляющее собой комбинацию обычного инсулина с цинком и белковым веществом протамином, медленнее всасывается и оказывает присущее инсулину действие на протяжении суток. Поэтому больной диабетом может вводить себе необходимую суточную дозу инсулина в одной инъекции, например утром.
Нельзя ли, однако, при лечении больных диабетом совсем отказаться от инъекций, т. е. вводить необходимое лекарственное вещество каким-либо иным способом?
Все попытки применять инсулин внутрь, через прямую кишку (в свечах или клизмах), под язык или вводя его в нос, оканчивались неудачей: инсулин или совсем не действовал, или его приходилось вводить в очень больших количествах, что значительно удорожало лечение. Поиски заменителей инсулина также не давали никаких результатов вплоть до 1955 года, когда было открыто, что некоторые сульфаниламидные препараты обладают инсулиноподобным действием и способны снижать у человека и животных содержание сахара в крови.
Такими препаратами являются нализан (относящийся к группе карбутамидов и известный также под названием BZ-55) и растинон (толбутамид D-860). В течение последних двух лет эти препараты были испытаны в лечебных учеждениях Германии, Англии, Франции, США и СССР более чем на 150 тыс. больных диабетом.
Оказалось, что эти препараты, принимаемые внутрь в виде таблеток, действительно способны заменять инъекции инсулина, но далеко не во всех случаях заболевания диабетом. Применение их эффективно преимущественно у больных старшей возрастной группы (40-45 лет), которые до перехода на лечение надизаном или растиноном нуждались в относительно небольших дозах инсулина (до 40 единиц в день). Подобные препараты не могут заменить инъекций инсулина при диабете, осложненном ацидозом, кожными проявлениями, диабетическими полиневритами, катарактой и пр.
Выяснилось также, что надизан оказывает при длительном применении нежелательные побочные действия (ухудшает функцию печени и отрицательно влияет на кровь). Значительно менее токсичен растинон, и поэтому в настоящее время большинство клиницистов применяет в тех случаях диабета, когда возможно использование сульфаниламидов, только последний препарат.
Следовательно, пока сделан только первый шаг к замене инъекций инсулина при лечении больных диабетом лекарствами, принимаемыми внутрь. Задачей эндокринологов является дальнейшее испытание соответствующих препаратов, которые были бы совершенно безвредны для человека и столь же активно действовали на углеводный обмен, как инсулин. Весьма вероятно, что такие препараты будут со временем найдены.
Гипогликемическая болезнь (гиперинсулинизм) стала известной всего около 30 лет назад и является в отношении причины, ее вызывающей, прямой противоположностью сахарного диабета. При гипогликемической болезни поджелудочная железа выделяет в кровь чрезмерное количество инсулина, в результате чего сахар в крови падает до ненормально низких цифр (состояние это называется гипогликемией).
Признаки гипогликемии хорошо известны, так как они могут наступать и у больных диабетом, если им введена слишком большая доза инсулина. Это резкое чувство голода, потливость, сердцебиение, дрожание конечностей, головокружение, наступление судорог и, наконец, бессознательное состояние.
Устранение гипогликемического состояния как при чрезмерном введении инсулина больным диабетом, так и у больных гипогликемической болезнью достигается сладким питьем или введением глюкозы внутривенно или под кожу. Обычно уже через несколько минут после введения глюкозы больной, впавший в бессознательное состояние, приходит в себя; содержание сахара в крови, которое во время приступа падает до очень низких цифр (20-30 мг%), возвращается к норме (80-120 мг%). Однако, так как приступы гипогликемии могут иногда повторяться по нескольку раз в день, больные гипогликемической болезнью вынуждены для их предупреждения употреблять очень много сахара (в некоторых наблюдавшихся нами случаях - до 500 г сахара ежедневно), в результате чего они очень полнеют. Часто повторяющиеся приступы гипогликемической болезни представляют угрозу для жизни больных.
Единственный способ радикального излечения гипогликемической болезни заключается в хирургическом вмешательстве, во время которого тщательно исследуется поджелудочная железа. Если при этом обнаруживают опухоль (аденому) поджелудочной железы, то удаление этой опухоли приводит к полному выздоровлению больных гипогликемической болезнью. При отсутствии опухоли причиной гипогликемической болезни может быть увеличение объема (гиперплазия) поджелудочной железы. В таких случаях производят частичное удаление ткани железы (резекцию), что также улучшает состояние больных.
Болезни гипофиза
Карликовый рост. Гигантизм и акромегалия. Болезнь Иценко-Кушинга. Несахарный диабет.
Гипофиз, или мозговой придаток, представляет собой небольшую железу размером меньше вишни. Вес ее у человека равен всего 0,5-0,7 г. Находится она у основания мозга и помещается в особом углублении черепа, известном под названием «турецкого седла».
Несмотря на небольшие размеры гипофиза, эта железа играет исключительно важную роль в жизнедеятельности организма. Она регулирует деятельность многих других желез внутренней секреции: надпочечников, половых желез, щитовидной и поджелудочной железы. Выделяемые гипофизом гормоны влияют на водно-солевой, жировой, углеводный и белковый обмен, на образование и выделение молока у кормящих женщин и многие другие функции организма. Деятельность гипофиза, в свою очередь, контролируется межуточным мозгом и корой головного мозга, с которыми он связан многочисленными нервными путями.
Раньше всего стала известна роль гипофиза как железы, регулирующей рост. Если удалить гипофиз у молодого животного, то оно перестает расти и остается карликом. При этом у животного не развивается половая система и оно лишается способности иметь потомство.
Такие же явления наблюдаются и у человека в тех случаях, когда имеется врожденное недоразвитие гипофиза или какая-нибудь инфекция, перенесенная в раннем детстве, вызвала повреждение гипофиза и нарушила нормальное образование в нем гормона роста. Такие дети растут очень медленно, они редко достигают 120-130 см даже к 18-20 годам, когда в норме рост человека прекращается. Заболевание это носит название гипофизарного карликового роста. У гипофизарных карликов мужского пола не растут борода и усы, половые органы остаются на детской ступени развития: они не могут иметь потомства. То же относится и к гипофизарным карлицам, у которых половая система не развивается (рис. 6).
| Рис. 6. 22-летняя девушка, страдающая гипофизарным карликовым ростом. Рост 122 см, вес 27 кг. Отсутствие вторичных половых признаков. Б, В - Когда Ваня пришёл в Институт детской эндокринологии, он был чуть выше 80 см и на много отставал от своих сверстников. За 6 лет лечения гормоном роста он вырос на 60-65 см и к 12-ти годам достиг роста 145 см. | ||
 |
 |
 |
В умственном отношении гипофизарные карлики развиваются нормально, чем они резко отличаются от тиреогенных карликов.
До революции нередко можно было видеть «труппы лилипутов» - гипофизарных карликов, гастролировавших на ярмарках, в цирках и балаганах. Хотя подлинные артистические дарования встречаются среди гипофизарных карликов не чаще, чем среди людей нормального роста, такие труппы карликов всегда пользовались успехом у зрителей, которым не приходило в голову, что перед ними выступают больные люди. В Советском Союзе, где образование стало общедоступным, многие гипофизарные карлики успешно оканчивают не только среднюю школу, но и высшие учебные заведения, получая возможность заниматься умственным трудом.
До недавнего времени лечение гипофизарных карликов было мало эффективно. Пробовали облучать у карликов малыми дозами рентгеновских лучей область гипофиза и межуточного мозга в надежде усилить выделение гормона роста, назначали прием небольших доз тиреоидина, пересаживали карликам под кожу гипофизы, взятые от животных, но все эти способы лечения если и увеличивали их рост, то в очень незначительной степени.
Лишь в последние годы был разработан метод пересадки таким больным гипофизов, взятых от людей, случайно погибших при различных несчастных случаях. Чтобы гипофиз, пересаженный карлику, скажем, в область плеча, прижился, сосуды гипофиза сшивают с кровеносными сосудами карлика. В 1956 году профессор Т. Е. Гнилорыбов сообщил об удачных пересадках гипофиза по этому методу, произведенных 11 гипофизарным карликам в хирургической клинике Днепропетровского медицинского института. В результате произведенных пересадок гипофизарные карлики выросли в течение 2-3 лет на 11-13 см.
Значительно сложнее лечение подобных карликов введением на протяжении нескольких лет гормона роста, получаемого из гипофизов животных. Этот гормон перед введением человеку нуждается в тщательной очистке; кроме того, он очень нестоек и при хранении быстро разрушается. Лечение недоразвития половой системы у гипофизарных карликов производится мужскими и женскими половыми гормонами.
Гигантский рост и акромегалия. Если вводить в течение длительного времени молодым животным, например щенкам или крысятам, вытяжки, или экстракты из гипофиза, то такие подопытные животные вырастают до гигантских размеров и превосходят по весу и росту в 2-3 раза нормальных животных того же возраста. Так, например, в результате ежедневных инъекций в течение года неочищенных экстрактов гипофиза, содержавших гормон роста, были выращены крысы весом от 700 до 900 г, тогда как нормальные крысы того же возраста весили только 300-450 г. Такие же гиганты-собаки были выращены из щенят, которым, начиная с семи недель, вводили ежедневно на протяжении 14 месяцев экстракты гипофиза, содержавшие гормон роста. Собаки-гиганты весили 44 кг, тогда как контрольные собаки того же помета (не получавшие гормон роста) весили в среднем 23 кг.
Таким образом, в опытах на животных была установлена несомненная зависимость гигантизма, изредка наблюдавшегося у человека, от повышенного выделения гипофизом гормона роста. Такие люди-гиганты описывались неоднократно.
Высшей границей нормального человеческого роста принято считать 180 см. Рост от 180 до 200 см условно признается за «субгигантизм», а свыше 2 м — за гигантский рост (Н. А. Шерешевский). Самый высокий точно установленный рост имел гигант, о котором сообщил Бушан, - 2 м 83 см.
Гигантизм, по современным представлениям, является болезнью, зависящей от чрезмерного выделения гипофизом гормона роста. Причиной этого может быть увеличение массы гипофизарной ткани или образование в гипофизе опухолей (эозинофильных аденом).
Близким к гигантизму заболеванием является акромегалия. Болезнь эта характеризуется возобновлением роста костной и других тканей у взрослого человека. Ввиду того что после периода полового созревания дальнейший рост в высоту невозможен (вследствие закрытия зон роста в длинных трубчатых костях), больные акромегалией растут преимущественно в ширину. При этом увеличиваются в размерах (утолщаются все кости скелета и ткани тела. Внутренние органы - сердце, печень, почки и др. - увеличиваются в 1,5-2 раза по сравнению с обычными. Даже волосы у больного акромегалией в 2 раза толще, чем у здорового человека. Особенно больших размеров достигают руки и ноги (акромегалия - название, составленное из греческих слов: «акрон» - конечность и «мегас» - большой), а также нижняя челюсть, нос и уши, в связи с чем, если заболевание возникло давно, диагноз может быть поставлен уже на основании одного внешнего вида больных (рис. 7).
При акромегалии рентгеновский снимок головы больного почти всегда позволяет обнаружить увеличение размеров турецкого седла, в котором, как указывалось, помещается гипофиз. Это увеличение вызывается опухолью гипофиза, состоящей из эозинофильных клеток (окрашивающихся в розовый цвет кислыми красками), которые выделяют гормон роста. Разрастающаяся опухоль гипофиза оказывает давление не только на стенки турецкого седла, но и на головной мозг, вследствие чего больные акромегалией часто жалуются на сильные головные боли, сопровождающиеся нередко тошнотами и рвотами. Непосредственно над гипофизом у человека находится перекрест зрительных нервов, и, если опухоль гипофиза сдавливает эти нервы, у больного акромегалией наступает значительное ухудшение, а затем и потеря зрения. В таких случаях необходимо удаление опухоли гипофиза.
У больных акромегалией мужчин снижаются половое чувство и потенция, у женщин почти всегда (у 87% больных) прекращаются месячные. При акромегалии нередко наблюдается усиление деятельности щитовидной железы и появление зоба (вследствие повышенного выделения гипофизом, помимо гормона роста, тиреотропного гормона, стимулирующего щитовидную железу). У части больных акромегалией развивается .
До последнего времени основным способом лечения акромегалии было облучение области гипофиза и межуточного мозга рентгеновскими лучами. Под их влиянием клетки опухоли гипофиза погибали и замещались соединительной тканью, вследствие чего приостанавливалось дальнейшее развитие болезни. При облучении принято было назначать больным по 100-200 рентгенов в день. За весь курс лечения, который длился от 15 до 30 дней в зависимости от того, проводилось ли облучение ежедневно или через день, больной получал 3-4 тыс. рентгенов. Лечение продолжалось 2-3 года, в течение которых больные акромегалией получали 4-5 курсов рентгенотерапии, а в общей сумме 12-15 тыс. рентгенов. Однако, несмотря на столь длительное лечение, далеко не у всех больных удавалось приостановить развитие болезни.
В 1952 году в скандинавском медицинском журнале появилось сообщение С. Джонсена о применении у 23 больных акромегалией видоизмененного метода рентгенотерапии. Этот врач довел ежедневную дозу облучения гипофизарномежуточной области до 600 рентгенов, а курс лечения сократил до 5 дней, в течение которых больные получали 3 тыс. рентгенов. Подобные курсы лечения он повторял 2-3 раза через каждые 2 месяца. После такой массивной рентгенотерапии, по утверждению Джонсена, наступило полное излечение почти у всех больных, наблюдавшихся им от 1 до 20 лет. У 15 больных в результате такого лечения стали менее выраженными внешние признаки акромегалии, а у пяти больных приостановилось дальнейшее увеличение конечностей (рис. 8).
| Рис. 7. Внешний вид больного акромегалией. Обращает на себя внимание увеличение нижней челюсти, ушей, носа. Рис. 8. Слева - больной акромегалией до начала рентгенотерапии. На правом снимке - он же через 8 лет после лечения массивными дозами рентгеновских лучей. | ||
 |
 |
 |
Эффективность лечения акромегалии массивными дозами рентгеновских лучей в настоящее время проверяется в ряде клиник как за рубежом, так и в СССР.
Болезнь Иценко-Кушинга. В 1932 году американский врач Кушинг описал болезнь, которая характеризуется ожирением лица и туловища (тогда как руки и ноги остаются относительно худыми), повышением кровяного давления, появлением на теле особых полос сине-багрового цвета и разрежением костного вещества, в результате чего кости теряют свою прочность. Кушинг приписывал болезнь появлению в гипофизе опухолей, состоящих из базофильных клеток (окрашивающихся в синий цвет основными красками). Однако еще в 1924 году советский невропатолог Н. М. Иценко описал то же заболевание, объяснив его возникновение изменениями в центрах межуточного мозга, которые регулируют работу гипофиза. Поэтому у нас принято называть данное заболевание по имени обоих описавших его авторов болезнью Иценко-Кушинга.
Заболевание это наблюдается у женщин значительно чаще, чем у мужчин. Лицо у больных приобретает округлую, «лунообразную» форму с багровым румянцем. Больные жалуются на слабость, сонливость, ухудшение памяти, боли в костях и особенно часто в позвоночнике; у женщин прекращаются месячные. На лице и туловище у женщин наблюдается усиленный рост волос (борода и усы пушкового типа), кожа сухая, шелушащаяся, на ней часто возникают гнойничковые сыпи и нарывы. У части больных развивается сахарный .
В связи с часто сопутствующим этой болезни повышением кровяного давления возникают вторичные заболевания почек, сердечно-сосудистой системы, печени и других органов, могут наступать самопроизвольные переломы костей (особенно часто - позвонков).
У части страдающих болезнью Иценко-Кушинга при тщательном клиническом обследовании удается обнаружить разрастание коры надпочечников или, как говорят врачи, гиперплазию, а иногда опухоли надпочечников. В таких случаях частичное оперативное удаление коры или извлечение опухоли надпочечника приводят к полному выздоровлению. В остальных случаях, когда причиной болезни являются изменения в межуточном мозге или опухоль гипофиза, применяется рентгеновское облучение головы и лечение половыми гормонами.
Несахарный диабет , или несахарное мочеизнурение, характеризуется нестерпимой жаждой и учащенным выделением мочи. Количество выпиваемой за сутки воды у больных несахарным диабетом, в зависимости от возраста и тяжести случая, колеблется в пределах от 3 до 15-20 л, но в отдельных, особенно тяжелых случаях может достигать огромных количеств - 30-40 л. Больные испытывают и днем, и ночью постоянную жажду, причем столь же часто ощущают потребность в опорожнении мочевого пузыря. В случаях резко выраженного несахарного диабета больные пьют каждый час, выпивая за раз до 1л воды или других жидкостей, и просыпаются до 10 раз за ночь из-за жажды и необходимости помочиться.
Больные несахарным диабетом обычно жалуются также на плохой аппетит, что, видимо, связано с большим количеством поглощаемой ими жидкости. В связи с этим больные быстро теряют в весе, иногда за короткий срок 8-10 кг. Если заболевание началось в детском возрасте, отмечается и отставание в росте вследствие хронического недоедания.
Потеря с мочой большого количества жидкости приводит к обезвоживанию тканей организма. Поэтому кожа у больных сухая, они почти не потеют даже при значительной физической работе. Отделение слюны понижено, возникает постоянное ощущение сухости во рту. Больные жалуются на зябкость, боли в суставах.
Мужчины болеют несахарным диабетом несколько чаще, чем женщины. Заболевание может возникнуть в любом возрасте: описаны случаи несахарного диабета даже у грудных детей 4-10 месяцев от роду. У детей старшего возраста болезни часто сопутствует ночное недержание мочи.
Опытами на животных и наблюдениями над больными людьми установлено, что несахарный возникает вследствие недостаточного выделения задней долей гипофиза антидиуретического гормона, препятствующего чрезмерной отдаче воды почками. Если человеку, страдающему несахарным мочеизнурением, впрыснуть под кожу вытяжку из задней доли гипофиза (питуитрин), то он на несколько часов перестает пить и мочиться. Действие однократной инъекции питуитрина продолжается, однако, всего 5-6 часов, а затем жажда возобновляется с прежней силой. Поэтому, чтобы устранить ее, больным несахарным диабетом приходилось вводить питуитрин три, а иногда и четыре раза в течение суток.
В 1935 году автор данной брошюры приготовил и впервые применил в СССР препарат для лечения несахарного диабета, названный им адиурекрином. Препарат этот, представляющий собой порошок, втягивается больными в нос, подобно нюхательному табаку, и избавляет их так же, как и питуитрин, на 5-6 часов от жажды. Таким образом, достаточно 3-4 понюшек адиурекрина в сутки, чтобы устранить все признаки болезни.
Адиурекрин изготовляют на мясокомбинатах из гипофизов крупного рогатого скота, овец, свиней и других животных. Придаток мозга при этом очищается от соединительной ткани, обезжиривается и затем измельчается в порошок. Втянутый в нос адиурекрин попадает на слизистую оболочку носа. Содержащийся в адиурекрине гормон всасывается слизистой носа, попадает в лимфатические пути и кровеносные сосуды и оказывает свое действие уже через 30 минут после того, как больной втянул в нос порошок.
За 20 с лишним лет применения адиурекрина в СССР препарат был испытан на сотнях больных несахарным диабетом. Почти во всех случаях он оказывает отличное лечебное действие, избавляя больных от необходимости делать уколы. Только изредка, когда у больных несахарным диабетом имеются атрофические изменения слизистой носа (так называемый атрофический ринит), препятствующие всасыванию адиурекрина, больным приходится прибегать к старому методу лечения - инъекциям питуитрина.
Как ни облегчает применение адиурекрина течение несахарного диабета, оно не устраняет причины болезни. Однажды возникнув, несахарный продолжается, за редкими исключениями, в течение всей жизни.
Каковы же причины, вызывающие появление несахарного диабета? Изучение обстоятельств, предшествующих заболеванию, показывает, что чаще всего появлению у больного жажды предшествовало заболевание гриппом, малярией, брюшным или сыпным тифом, сифилисом или какой-либо другой инфекцией. Изредка причиной болезни может быть травма черепа, вызвавшая кровоизлияние в мозг.
При вскрытии людей, страдавших при жизни несахарным диабетом, находили в гипофизе или межуточным мозге рубцы или другие изменения, которые нарушили нормальное выделение гипофизом антидиуретического гормона. Лишь в редких случаях начатое тотчас после перенесенного гриппа, малярии и других заболеваний лечение пенициллином, стрептомицином, хинином и другими антибиотиками и лекарствами может предотвратить наступление стойких изменений в гипофизе или межуточном мозге и излечить несахарный .
Делались попытки излечить больных несахарным диабетом путем пересадки им под кожу гипофизов, взятых от различных животных, вплоть до обезьян. До сих пор все такие попытки не увенчались успехом; через 2-3 недели гипофиз, пересаженный больному, рассасывался и вновь возникала жажда и учащенное мочеиспускание. Возможно, что в будущем удастся усовершенствовать операцию пересадки гипофиза на сосудистой ножке подобно тому, как это стали делать гипофизарным карликам. Это позволит радикально излечивать людей, страдающих несахарным диабетом.
Надпочечники и их заболевания
Аддисонова или бронзовая болезнь. Гормоны надпочечников и их лечебное применение. Нарушения выработки надпочечниками половых гормонов.
Надпочечники представляют собой небольшие железы внутренней секреции, расположенные непосредственно над почками, к которым они тесно прилегают. Вес одного надпочечника у человека равен всего 5-7 г; формой своей он напоминает треугольник и состоит из двух слоев ткани, носящих название мозгового и коркового слоя. Несмотря на небольшую величину надпочечников, выделяемые ими гормоны играют исключительно важную роль в поддержании нормальной жизнедеятельности организма. Без надпочечников жизнь человека и животных невозможна. Лишенные оперативным путем обоих надпочечников животные погибают в течение нескольких суток.
Частичное нарушение деятельности надпочечников ведет к развитию у человека тяжелого заболевания, известного под названием бронзовой или аддисоновой болезни (по имени впервые описавшего ее врача). В восьми случаях из десяти аддисонова болезнь возникает вследствие разрушения большей части надпочечников туберкулезом. При бронзовой болезни развивается крайняя общая слабость, исхудание, понижение кровяного давления; кожа больных приобретает своеобразную коричневато-черную окраску, напоминающую цвет бронзы. Эта окраска кожи особенно заметна в области пояса и на других участках тела, которые подвергаются трению одежды. На языке, внутренней поверхности щек и на деснах также появляются коричневые или черные пятна. Очень часто болезни сопутствуют желудочно-кишечные расстройства, которые еще больше истощают больных.
Возникает аддисонова болезнь обычно в возрасте от 30 до 50 лет, причем несколько чаще ею болеют мужчины. Еще недавно эффективных средств лечения этой болезни не существовало. В настоящее время положение коренным образом изменилось.
В 1931 году был изготовлен экстракт коры надпочечников - кортин, систематическое введение которого позволило поддерживать жизнь животных с удаленными надпочечниками. В 1936 году был получен еще более активный гормон этой железы - кортизон; наконец, в 1938 году из коры надпочечников был выделен гормон, влияющий на водно-солевой обмен и повышающий кровяное давление, - дезоксикортикостерон. Применение этих гормональных препаратов при лечении аддисоновой болезни дает поразительные результаты. Систематическое введение кортизона в ничтожных количествах - всего от 12,5 до 25 мг в день - преображает больных аддисоновой болезнью: исчезает темная окраска кожи, восстанавливается мышечная сила, возвращается к норме кровяное давление, прекращаются тошноты, рвоты и поносы, больные прибавляют в весе; многие больные, превратившиеся в полных инвалидов, вновь возвращаются к трудовой деятельности.
Двадцать лет назад длительность жизни заболевших тяжелой формой аддисоновой болезни обычно не превышала двух-трех лет, а иногда смерть наступала уже через несколько месяцев после начала заболевания. Теперь же люди, страдающие аддисоновой болезнью, живут десятилетиями, сохраняя при этом хорошее самочувствие и работоспособность. Женщины, страдающие аддисоновой болезнью, могут теперь иметь детей. Известно уже много случаев беременности и благополучных родов у таких больных.
За последние годы стало известно много новых фактов, свидетельствующих об исключительном значении надпочечников в защите организма человека от любых вредных воздействий. Так, установлено, что при заражении инфекционной болезнью, ранениях, ушибах, ожогах, обморожениях, поражении электрическим током и т. п. под влиянием импульсов, поступающих из центральной нервной системы, происходит быстрое, в течение нескольких часов, увеличение объема надпочечников и соответствующее усиление их работы. При этом надпочечники начинают выделять в кровь большое количество гормонов, повышающих сопротивляемость организма любым вредным воздействиям, в частности, помогающих ему справиться с инфекцией. Если тяжелое заболевание длится долго, может наступить истощение усиленно работающих надпочечников, и человек погибает при явлениях надпочечниковой недостаточности.
Эти наблюдения послужили основой для использования гормонов надпочечников не только при бронзовой и других болезнях, связанных с нарушением нормальной работы надпочечников, но и при иных заболеваниях. Так, адреналин и дезоксикортикостерон, повышающие кровяное давление, позволяют теперь спасти жизнь людей, находящихся в состоянии шока или коллапса. Применение кортизона или адрено-кортикотропного гормона гипофиза (АКТГ) дает поразительный эффект при многих болезнях, ранее трудно поддававшихся лечению.
В 1949 году кортизон был впервые применен для лечения острого суставного ревматизма, а также анкилозирующего полиартрита - заболевания, при котором воспаление суставов делает их тугоподвижными, а затем полностью лишает человека возможности двигаться, т. е. превращает его в полного инвалида, который годами прикован к постели и не может двигать ни руками, ни ногами.
Если лечение кортизоном начато своевременно, опухоль суставов уже через 2-3 дня спадает и температура понижается до нормы; постепенно восстанавливается и подвижность в пораженных суставах. При остром ревматическом воспалении суставов раннее применение кортизона или АКТТ, но наблюдениям советских врачей, уменьшает количество осложнений (поражения сердечных клапанов и пр.).
Кортизон или АКТГ во многих случаях устраняют на несколько недель или месяцев приступы бронхиальной астмы. Эти же препараты с успехом применяют при подагре, язвенных колитах, некоторых глазных и кожных болезнях. При обширных ожогах кортизон спасает жизнь людей, в прошлом считавшихся обреченными.
Получение кортизона из надпочечников животных (коров, овец, свиней) очень трудоемко и дорого: из одной тонны надпочечников получают меньше одного грамма кортизона. Поэтому трудно переоценить значение разработанного в настоящее время химиками метода синтетического получения кортизона из различных веществ животного и растительного происхождения.
Производство этого гормонального препарата в неограниченном количестве имеет исключительное значение для повышения эффективности лечения многих заболеваний.
Нарушения выработки надпочечниками половых гормонов. Кроме гормонов, о которых мы уже упоминали, кора надпочечников выделяет в кровь мужские и женские половые гормоны. При гиперплазии надпочечника или образовании в нем опухоли выработка половых гормонов резко повышается. В таких случаях у детей может наступить раннее половое созревание. У мужчин наблюдается феминизация (развитие женского облика), а у женщин - вирилизация (развитие мужеподобности). Заболевание это значительно чаще встречается среди женщин.
Признаки подобного заболевания, называемого надпочечниково-половым синдромом, следующие: у здоровой до того женщины начинают расти борода и усы, появляются волосы на груди, животе и ногах, атрофируются молочные железы» прекращаются месячные. Внешний облик больной изменяется - вместо мягких, округлых линий, свойственных женской фигуре, развивается мускулистый мужской торс. Меняется и голос, приобретающий низкий мужской тембр. На больных угнетающе действует необходимость постоянно уничтожать растущие на лице волосы, чтобы не привлекать внимания окружающих.
Задача врача в таких случаях заключается в том, чтобы установить, вызвано ли заболевание действительно опухолью надпочечников, так как очень схожие заболевания могут возникать и при опухолях яичника или наличии изменений в межуточном мозге и гипофизе. Чтобы выяснить, какая железа внутренней секреции повинна в возникновении мужеподобности у женщины, производят всестороннее обследование больной: делают рентгеновский снимок надпочечников после введения в околопочечные ткани кислорода, исследуют содержание в моче так называемых 17-кетостероидов - продуктов обмена гормонов надпочечников (при опухолях надпочечников выделение их с мочой значительно увеличивается); производят также снимки черепа, повторные гинекологические исследования к т. д.
После того как установлено, в каком надпочечнике находится опухоль (левом или правом), ее удаляют хирургическим путем. Через некоторое время больные выздоравливают (рис. 9).
| Рис. 9. Слева — 39-летняя женщина с мужеподобной внешностью. Справа — та же женщина через 11 месяцев после удаления опухоли левого надпочечника, достигавшей размеров крупного мандарина. | ||
 |
 |
 |
Еще недавно такие операции были сопряжены с большим риском, так как при наличии опухоли в одном из надпочечников второй надпочечник находится в недеятельном (атрофическом) состоянии. Поэтому при удалении опухоли надпочечника больные часто умирали от острой надпочечниковой недостаточности. Теперь благодаря открытию кортизона эта опасность миновала: с первого же дня после операции больные получают кортизон и чувствуют себя отлично. Через 7-8 дней после операции введение кортизона прекращают. К этому времени оставшийся у больного второй надпочечник начинает вырабатывать в достаточном количестве соответствующий гормон.
Множественные заболевания эндокринных желез
Ожирение и истощение. Преждевременное половое созревание. Преждевременная старость.
В этом разделе мы остановимся на нескольких заболеваниях, зависящих от нарушения деятельности одновременно двух или более желез внутренней секреции.
Примером такого заболевания является болезнь Фрёлиха, впервые описавшего ее в 1901 году, или адипозо-генитальная дистрофия. Первым бросающимся в глаза признаком этой болезни является чрезмерное больных, вес которых может достигать 150-180 кг и более.
Следует заметить, что не всякое говорит о наличии болезни Фрёлиха. Нередко можно встретить чрезмерно полных, страдающих ожирением людей, особенно среди лиц, не занимающихся физическим трудом. Это так называемое экзогенное , т. е. от внешних причин, связанное преимущественно с нерациональным питанием (переедание, чрезмерно высокая по калорийности пища) и недостаточным расходом физической энергии.
Таким образом, болезнь Фрёлиха представляет собой результат нарушения деятельности нескольких желез внутренней секреции; поэтому и лечение этой болезни - комплексное, заключающееся во введении многих препаратов - гормонов половых желез, гипофиза и щитовидной железы. Если у больных обнаружена опухоль мозга или гипофиза, назначают лечение рентгеновскими лучами как при акромегалии или же удаляют опухоль оперативным путем. Помимо этого при болезни Фрёлиха полезны и общие мероприятия, которые проводятся при любом виде ожирения: с ограничением ной пищи и легко усвояемых углеводов (сахара, сладостей, мучнистых блюд), разгрузочные дни, назначаемые 1-2 раза в неделю (в такие дни больной получает 1-1,5 кг фруктов или такое же количество молока или кефира), а также различные физиотерапевтические методы лечения (лечебная гимнастика, водолечение и пр.).
Противоположностью болезни Фрёлиха по действию на жировой обмен является болезнь Симмондса, впервые описавшего ее в 1914 году, или гипофизарная кахексия. При этой болезни наблюдается крайняя степень похудания, больные теряют половину первоначального веса и более; волосы у них выпадают на всем теле, развивается общая слабость, полное физическое истощение, при котором даже самая легкая работа становится непосильной; у женщин прекращаются месячные, у мужчин падает половая способность. Кровяное давление при этой болезни значительно понижается, падает и уровень сахара в крови, температура тела на 1-2 градуса ниже нормальной. Кожа у больных чрезвычайно сухая, отмечается выпадение зубов.
Болезнь Симмондса развивается на почве уменьшения размеров (атрофии) передней доли гипофиза в результате кровоизлияний или воспалительных процессов после тифа, гриппозной, сифилитической и других инфекций. Нарушение деятельности гипофиза влечет за собой понижение функции половых желез, надпочечников, щитовидной железы.
До недавнего времени лечение болезни Симмондса было мало успешным. Только в случаях, вызванных сифилисом или туберкулезом, можно было рассчитывать на улучшение состояния больных, если противосифилитическое или противотуберкулезное лечение производилось на ранних стадиях болезни. В настоящее время, когда имеются активные гормональные препараты гипофиза, половых желез и надпочечников, лечение данного заболевания подобными препаратами дает хорошие результаты.
Преждевременное половое созревание характеризуется появлением в детском возрасте признаков, свойственных взрослым мужчинам и женщинам. Нормально в нашем климате половое созревание начинается в 12-13 лет и полностью заканчивается к 18-20 годам. При преждевременном половом созревании детей в 5-7-летнем возрасте или еще раньше начинается рост половых органов и развитие вторичных половых признаков. У девочек увеличиваются молочные железы, появляется оволосение лобка и подмышечных впадин, могут начаться месячные. У мальчиков начинается преждевременный рост усов и бороды, а половые органы достигают размеров свойственных взрослым мужчинам. При раннем половом созревании дети обычно значительно обгоняют в росте сверстников. Так, например, у девочки 4½ лет с хорошо развитыми молочными железами, наличием оволосения лобка и регулярными месячными, рост равнялся 117 сантиметрам, т. е. соответствовал росту 8-летней девочки. Мальчик, у которого в 7-летнем возрасте началось преждевременное развитие половой системы, имел в 9 лет рост 1 м 52 см. Он выглядел как 18-летний юноша и говорил басом. Однако в дальнейшем такие дети перестают расти, и в конечном итоге рост их не превышает среднего роста взрослого человека.
Различают две формы раннего полового созревания детей. При одной из них наблюдается только преждевременное физическое и половое развитие, психика же и поведение остаются на детской ступени. При второй - преждевременному физическому и половому развитию сопутствует раннее развитие умственных способностей.
Причины раннего полового развития детей разнообразны. Чаще всего - это опухоли половых желез (семенников у мальчиков и яичников у девочек), причем эти опухоли могут быть злокачественными. При этом железы вырабатывают избыточное количество половых гормонов, под влиянием которых вторичные половые признаки развиваются раньше нормального срока. Раннее половое созревание может наступить также при опухолях надпочечников, шишковидной железы (эпифиз), водянке головного мозга и при опухолях в межуточном мозге или в непосредственном соседстве с гипофизом. Возможно, что при опухолях мозга механическое давление, оказываемое ими на гипофиз, вызывает усиленное выделение гонадотропных гормонов, стимулирующих раннее развитие половых органов.
Преждевременное половое развитие легко получить в экспериментах на животных, если вводить им гонадотропные гормоны, полученные из передней доли гипофиза. Изредка раннее половое развитие детей объясняется наследственностью и не представляет собой болезни в прямом смысле этого слова.
В каждом случае раннего полового созревания необходимо производить тщательное клиническое обследование детей, чтобы установить причину его возникновения. Если обнаруживается опухоль (как уже указывалось, иногда злокачественная), ее, разумеется, следует удалить хирургическим путем как можно раньше. В таких случаях признаки раннего полового созревания быстро исчезают: у мальчиков выпадает борода и усы и уменьшаются в размерах половые органы, у девочек прекращаются месячные и подвергаются обратному развитию молочные железы. В дальнейшем такие дети развиваются нормально.
Раннее старение. Это редкое эндокринное заболевание связано с одновременным нарушением деятельности многих желез внутренней секреции. В случае, описанном доктором Н. И. Цыгановой, 16-летняя девушка выглядела как пожилая женщина 50 лет (рис. 10).
| Рис. 10. Преждевременное постарение у 16-летней девушки. Б — Казах 24-х лет. В — Женщина 30-ти лет. | ||
 |
 |
 |
Преждевременное старение может быть следствием склероза сосудов, снабжающих кровью железы внутренней секреции. Наступающее при этом ухудшение питания эндокринных желез снижает количество вырабатываемых ими гормонов. В свою очередь, явления склероза могут быть вызваны хронической инфекцией (сифилис, малярия и пр.). Поэтому терапия раннего старения заключается, с одной стороны, в лечении основной болезни и, с другой, - в постоянном введении недостающих в организме гормонов гипофиза, щитовидной железы, надпочечников и половых желез.
Половые железы и их заболевания
Мужские и женские половые гормоны. Лечение недостаточности половых желез.
Половые железы - семенники у мужчин и яичники у женщин - это парные органы, выделяющие в кровь половые гормоны, влияющие на развитие вторичных половых признаков. Мужские половые гормоны вызывают рост бороды и усов, от наличия этих гормонов зависит развитие свойственной мужчине мускулатуры, развитие полового органа, низкий мужской голос. Женские половые гормоны влияют на развитие молочных желез, рост матки, характерное для женской фигуры отложение жировой ткани в определенных местах тела.
Изменения, наступающие в развитии человека, лишенного половых желез в детском возрасте, были хорошо изучены в прошлом веке при обследованиях секты скопцов, существовавшей в царской России. Представители этой религиозной секты считали, что люди, живущие половой жизнью, впадают в «грех». Чтобы обеспечить себе место в раю, члены секты взаимно оскопляли (кастрировали) друг друга, подвергая этой операции и детей, у которых с годами появлялось так называемое евнухоидное телосложение, для которого характерны высокий рост и нарушение пропорций тела за счет непомерного удлинения ног. Заметно увеличивалась и длина рук. У юношей-кастратов сохранялся высокий, детский тембр голоса, усы и борода не росли, половые органы оставались на детской ступени развития. У девушек-кастратов не развивались молочные железы, отсутствовали месячные; они становились неспособными к зачатию.
Подобные изменения в росте и развитии наблюдаются и в тех случаях, когда у ребенка имеется врожденное недоразвитие половых желез или если в раннем детском возрасте в результате воспалительных процессов или ранений половые железы оказались недеятельными. Это заболевание носит название евнухоидизма.
Если удалить половые железы у взрослого человека, уже после полового созревания (врач вынужден делать это при туберкулезе или злокачественных опухолях половых желез, их ранениях), а также если эти железы перестали выделять половые гормоны вследствие происшедших в них воспалительных изменений, то картина заболевания будет несколько иной. Влияния на рост кастрация не окажет, но во внешнем облике и психическом состоянии больного обнаружатся значительные изменения.
У мужчин после кастрации замедляется или совсем прекращается рост бороды и усов, уменьшаются размеры половых органов, наступает частичная или полная импотенция (неспособность к половой жизни). У женщин прекращаются месячные, уменьшаются молочные железы, возникают тягостные ощущения жара и потливости (приливы). Кастрация вызывает изменения и в нервно-психической сфере: повышенную нервную возбудимость, неуравновешенность, периоды депрессии (угнетенного настроения), ухудшение памяти и работоспособности.
При частичном поражении половых желез в результате воспалительного заболевания характерные для кастрации явления не возникают, но, в зависимости от степени понижения выработки железами половых гормонов, отмечаются более или менее выраженные признаки их недостаточности. Подобное состояние называется гипогенитализмом.
До недавнего времени врачи не располагали активными средствами, с помощью которых можно было бы устранять последствия кастрации или гипогенитализма. В настоящее время такие активные гормональные препараты имеются.
В 1931 году из мочи человека был выделен первый мужской половой гормон - андростерон, а в 1935 году из семенников быка был получен еще более активный гормон - тестостерон, различные соединения которого и применяются в настоящее время для лечения.
В период с 1929 по 1935 год были открыты четыре женских половых гормона: эстрон, эстриол, эстрадиол и прогестерон (гормон желтого тела). С помощью этих гормональных препаратов можно устранять ненормальности развития и болезненные явления, зависящие от недостаточности половых желез у женщин.
Из женских половых гормонов широко используются фолликулин, вводимый в инъекциях, и синтетические препараты - синэстрол и диэтилстилбэстрол, применяемые в таблетках внутрь, а также в инъекциях. Три перечисленных женских гормональных препарата представляют собой эстрогены, т. е. вещества, способные восстанавливать течку («эструс») у кастрированных самок животных.
Столь же эффективно применение и мужских половых гормонов. Наш опыт лечения мужчин, которые были кастрированы по медицинским показаниям (ранения в паховую область с размозжением половых желез), показал, что для восстановления половой потенции и вторичных половых признаков достаточно вводить больным мужской половой гормон (тестостерон-пропионат) в дозе 20 мг в неделю. Иными словами, чтобы заменить функцию отсутствующих половых желез у взрослого мужчины, требуется в течение года всего около 1 г тестостерон-пропионата.
Тестостерон-пропионат вводят внутримышечно путем инъекций. Существует и другой препарат мужского полового гормона - метилтестостерон, принимаемый в таблетках, помещаемых под язык. Медленно растворяясь, гормон, заключенный в таблетке, всасывается слизистой оболочкой рта и по лимфатическим путям поступает в кровь.
Больным, которые нуждаются в длительном лечении половыми гормонами (при евнухоидизме, кастрации), делают подсадку таблеток гормона. Для этого пользуются шприцем особой конструкции, в который закладывают маленькие таблетки гормона. Через иглу с широким отверстием такая таблетка вводится, например, под кожу живота, образуя здесь своеобразное «гормональное депо», из которого, по мере растворения таблетки, гормон медленно всасывается и поступает в кровь. Действие одной такой «подсадки» длится от 4 до 6 месяцев, так что повторять их необходимо не чаще 2-3 раз в год.
При лечении как у мужчин, так и у женщин гипогенитализма требуются значительно меньшие количества гормональных препаратов, чем при полном отсутствии половых желез.
В возрасте 45-50 лет, когда у большинства женщин наступает угасание деятельности половых желез и прекращаются месячные (климакс), может развиться состояние, характеризующееся повышенной нервной возбудимостью, ухудшением сна, чувством онемения в кистях рук, частыми приливами. В то время как у большинства женщин климактерический период протекает без каких-либо признаков ухудшения самочувствия, некоторые переносят его очень тяжело. Устранение подобных проблем достигается приемом небольших доз эстрогенов (например, синэстрола в таблетках). Следует отметить, что принимать эстрогенные препараты по поводу климактерических расстройств можно только после гинекологического осмотра, с разрешения врача. При наличии фибромы или фибромиомы матки эстрогенные гормоны принимать нельзя, так как они усиливают рост этих опухолей.
Применение гормональных препаратов при различных заболеваниях
На заре эндокринологии для лечебных целей применялись водные, спиртовые или глицериновые вытяжки (экстракты) из желез животных или непосредственно измельченные ткани эндокринных желез. В таких органотерапевтических препаратах в большинстве случаев содержалось ничтожное количество гормонов, и потому лечение ими было мало успешно.
Современные органопрепараты подвергаются сложной обработке и очистке от примесей, вследствие чего они становятся гораздо активнее. Благодаря успехам современной химии многие гормоны добываются теперь не из желез животных, а синтетически, причем по своему действию они ничем не отличаются от натуральных гормонов.
Все гормональные препараты, поступающие в продажу, предварительно стандартизуются, т. е. проходят проверку в государственных контрольных лабораториях, где препараты испытываются на животных; активность каждого гормонального лекарства обозначается на этикетках в стандартных международных «единицах действия». Так, например, за единицу действия женского полового гормона (эстрогена) принимается то количество препарата, которое восстанавливает течку у самки мыши, подвергнутой кастрации; единицей действия инсулина считается то количество этого гормона, которое понижает содержание сахара в крови у кролика наполовину (с 90 до 45 мг%) и т. д.
Разностороннее влияние, оказываемое гормональными препаратами на процессы обмена в организме, используется в настоящее время для лечения не только эндокринных, но и иных заболеваний. Ниже приведены краткие сведения о применении гормональных препаратов при некоторых из этих заболеваний.
Болезненные месячные, не связанные с воспалительными заболеваниями в малом тазу. При так называемой дисменоррее - месячных, протекающих с значительными болями, лечебное действие оказывает гормон желтого тела (прогестерон), назначаемый в инъекциях по 0,005, или его заменитель - прегнин, применяемый по три таблетки два раза в день под язык. Действие гормона желтого тела при дисменоррее объясняется тем, что он понижает возбудимость мышц матки и ослабляет ее сокращения, вызывающие боли. Прогестерон или прегнин принимают в течение 6-7 дней до ожидаемого срока месячных по назначению гинеколога и под его наблюдением.
Бронхиальная астма. Кроме кортизона и АКТГ, о применении которых при бронхиальной астме уже сообщалось, хорошие результаты при этом заболевании дает введение паратиреокрина - препарата, получаемого из околощитовидных желез животных. Паратиреокрин обладает способностью повышать содержание кальция в крови, что устраняет спазм бронхиол (мельчайших разветвлений бронхов в легких) и прекращает приступы астмы. Паратиреокрин вводится подкожно по 2 мл ежедневно в течение 10-15 дней.
Ночное недержание мочи у детей. При этом заболевании во многих случаях хорошее действие оказывает адиурекрин. Препарат втягивают в нос (в обе ноздри) один раз в день, непосредственно перед сном. Доза для детей до 10 лет - 0,02. Действие адиурекпина при ночном недержании мочи объясняется тем, что он повышает тонус сфинктера (запирающей мышцы) мочевого пузыря. При лечении адиурекрином необходимо следить за тем, чтобы дети перед сном обязательно опорожнили мочевой пузырь. В большинстве случаев применение адиурекрина в течение 2-3 недель избавляет ребенка от этого недуга.
Общее истощение. При пониженном питании, связанном с плохим аппетитом, которое нельзя объяснить каким-либо общим заболеванием, применяют инъекции инсулина под кожу по 4-6 единиц один или два раза в день. Инсулин вызывает понижение сахара в крови, в связи с чем рефлекторно возникает чувство голода и появляется хороший аппетит. Инсулин следует вводить за 10-15 минут до еды, причем, если после инъекции нет возможности плотно позавтракать или пообедать, обязательно нужно съесть 4-5 кусочков сахара во избежание наступления гипогликемии (см. стр. 18). Курс инсулинотерапии при истощении продолжается 20-30 дней. До и после окончания курса лечения рекомендуется взвеситься, чтобы знать, насколько увеличился вес.
Ожирение. Наряду с диетой (ограничение мучнистых и жирных блюд), разгрузочными днями, водолечением и физическими упражнениями уменьшение веса тела при ожирении достигается применением тиреоидина. Лечение это должно проводиться обязательно под наблюдением врача. Некоторые’ люди, страдающие ожирением, длительное время хорошо переносят прием тиреоидина в больших дозах - по 0,4-0,6 в день, тогда как у других введение этого препарата даже в малых дозах (0,1) уже через несколько дней вызывает сердцебиение, потливость, ухудшение сна, в связи с чем прием тиреоидина приходится прерывать или прекращать вовсе.
Язва желудка или двенадцатиперстной кишки. Женские половые гормоны обладают сосудорасширяющим действием и улучшают кровоснабжение тканей, способствуя тем самым заживлению язв, ран, ссадин и других нарушений целостности тканей тела. На этом свойстве женских половых гормонов основано их применение как у мужчин, так и у женщин при язвенной болезни желудка или двенадцатиперстной кишки. Один из эстрогенных препаратов - фолликулин, синэстрол или диэтилстилбэстрол вводят внутримышечно по 10-20 тысяч единиц в течение 2-3 недель. У значительного числа больных это лечение, даже без применения диеты, устраняет боли и приводит к рубцеванию язвы.
Такие же хорошие результаты дает лечение длительно незаживающих, так называемых трофических язв на поверхности тела (часто на голенях) фолликулиновой мазью (5 тысяч единиц фолликулина или синэстрола на 15 г вазелина или ланолина). При наложении в течение нескольких недель повязок с такой мазью (повязки меняют 2 раза в неделю) у многих больных наступает заживление язв, не поддававшихся до того лечению в течение ряда месяцев. Трещины сосков у кормящих матерей при применении в течение 7-10 дней той же фолликулиновой мази почти во всех случаях заживают полностью. При недоразвитых и втянутых сосках местное применение фолликулиновой мази полезно и в предродовом периоде для подготовки молочных желез к кормлению, так как эстрогенные гормоны способствуют развитию сосков.
Мы рассказали о некоторых заболеваниях желез внутренней секреции и новых методах их лечения. Разумеется, в небольшой научно-популярной брошюре невозможно затронуть все известные эндокринные заболевания, а тем более подробно рассказать о них. Это потребовало бы значительного увеличения объема брошюры. По этой причине мы не привели сведений о других видах карликового роста, кроме вызываемых болезнями гипофиза и щитовидной железы, не описали болезней, связанных с недостаточностью околощитовидных желез (тетания и пр.), а также о некоторых других сравнительно редких эндокринных заболеваниях. В разделе о применении гормональных препаратов при различных заболеваниях дан обзор только некоторых из них, наиболее часто встречающихся. Однако даже те сведения, которые получит читатель из данного научно-популярного очерка, убедят его в том, что медицинская наука и, в частности, одна из ее отраслей - эндокринология, движется вперед быстрыми темпами, увеличивая год от года могущество человека в борьбе с самыми различными заболеваниями.
ГЛАВА 6. ЖЕЛЕЗЫ ВНУТРЕННЕЙ СЕКРЕЦИИ (эндокринные железы)
В организме человека имеется две системы желез. Одни железы, например, пищеварительные, имеют протоки, которые открываются в полость пищеварительного тракта, куда изливается секрет этих желез. Другие железы не имеют выводных протоков. Их секрет поступает непосредственно в кровь. Поэтому первые называют железами внешней секреции, а вторые - внутренней секреции , или эндокринными железами (рис. 366).
Рисунок 366. Положение эндокринных желез в теле человека. Вид спереди. I – гипофиз и эпифиз; 2 – паращитовидные железы; 3 – щитовидная железа; 4 – надпочечники; 5 -панкреатические островки; 6 – яичник; 7 – яичко.
Важное значение в жизнедеятельности человека и животных имеют биологически активные вещества - гормоны. Они вырабатываются особыми железами, которые богато снабжены кровеносными сосудами. Эти железы не имеют выводных протоков, и их гормоны поступают непосредственно в кровь, а затем разносятся по всему телу, осуществляя гуморальную регуляцию всех функций: они возбуждают или угнетают деятельность организма, влияют на его рост и развитие, изменяют интенсивность обмена веществ. В связи с отсутствием выводных протоков эти железы называются железами внутренней секреции, или эндокринными, в отличие от пищеварительных, потовых, сальных желез внешней секреции, имеющих выводные протоки.
По строению и физиологическому действию гормоны специфичны: каждый гормон оказывает мощное влияние на определенные процессы обмена веществ или работу, органа, вызывая замедление или, наоборот, усиление его функции. К железам внутренней секреции относятся гипофиз, щитовидная железа, околощитовидные железы, надпочечники, островковая часть поджелудочной железы, внутрисекреторная часть половых желез. Все они функцио-нально взаимосвязаны между собой: гормоны, вырабатываемые одними железами, оказывают влияние на деятельность других желез, что обеспечивает единую систему координации между ними, которая осуществляется по принципу обратной связи. Главенствующая роль в этой системе принадлежит гипофизу, гормоны которого стимулируют деятельность других желез внутренней секреции.
Нервная и эндокринная системы связаны теснейшим образом, и их можно рассматривать как часть единой системы, координирующей органические функции и поддерживающей постоянство внутренней среды. Первая воспринимает внешние раздражители и генерирует ряд


Рисунок 367. Гормональная связь. Рисунок 368. Нервная связь.
ответных реакций. Вторая представляет собой систему внутреннего контроля и регуляции, компенсирующую изменения, внесенные извне.
Обе используют химические агенты: нервная система использует нейромедиаторы - молекулярные сигналы, идущие от одной нервной клетки к другой благодаря электроимпульсу; эндокринная состоит из ряда клеток, организованных в железы, выделяющие гормоны в кровь для доставки в места, где они должны выполнять свои функции.
Гормональная система - система медленного действия, в то время как нервная система обладает намного более быстрой ответной реакцией.
Многие насекомые и рыбы выделяют гормоны, адресованные особям своего вида. Эти химические послания, отправляемые во внешнюю среду, - феромоны - вызывают различные ответные реакции у адресата: действуют как призыв к спариванию, сигнал тревоги.
Например, пчелиные матки выделяют феромон, который, будучи поглощенным рабочими пчелами, препятствует тому, чтобы какая-либо из них могла произвести другую матку.
Другие феромоны могут служить следом, направляющим особей какого-либо сообщества туда, где есть пища, что характерно для муравьев.
Один из самых сильных феромонов у бабочки шелкопряда - он действует как призыв к спариванию, и достаточно нескольких сотен его молекул, чтобы вызвать ответную реакцию самца.
Гормоны, вырабатываемые эндокринными железами, выделяются в кровоток и поступают во все части организма, но каждый из них действует только в одном месте или в определенном органе тела, именуемом органом-мишенью .
Полагают, что гормоны опознают свой орган-мишень благодаря наличию неких белков-рецепторов. Гормоны обнаруживают их и соединяются с ними для влияния на клетки и ткани. Это влияние может проявляться в разных формах. Некоторые гормоны, такие, как инсулин и глюкагон, побуждают клетки на выработку определенных соединений - это то, что известно как динамическое влияние .
Другие оказывают метаболическое влияние : ускоряют или замедляют обмен веществ в определенных клетках.
Гормон роста оказывает морфогенетическое влияние , так как стимулирует развитие и дифференциацию клеток в некоторых органах тела.
Химическая природа гормонов
Гормональные жидкости имеют химическую природу, которая обеспечивает совершенное взаимодействие различных органов тела человека. Английские ученые Старлинг и Бейлисс, открывшие эти жидкости в 1906 г., назвали их гормонами , учитывая этимологию греческого слова hormao, что значит возбуждать, стимулировать .
Гормоны могут соответствовать нескольким типам органических молекул.
Белки с короткой цепью : состоят из немногих аминокислот, например, окситоцин и вазопрессин.
Белки с длинной цепью : состоят из многих аминокислот, например, инсулин и глюкагон.
Производные жирных кислот : например, простагландины.
Производные аминокислот : такие, как адреналин и тироксин.
Стероиды : такие, как половые гормоны и гормоны, выделяемые корой надпочечников.
Таблица 16. Железы внутренней секреции
|
Располо-жение |
Строение |
Воздействие на организм |
||||
|
гиперфункция (избыточное действие) |
гипофункция (недостаточное действие) |
|||||
|
Ниже моста головного мозга |
Мозговой придаток, состоящий из трех частей: передней, проме-жуточной и задней доли |
Ростовые |
Регулируют рост орга-низма в мо-лодом воз-расте |
В молодом воз-расте вызывают гигантизм, у взро-слых – болезнь акромегалию |
Задерживают рост (кар-ликовость), при этом пропорции тела и умст-венное развитие остаются нормальными |
|
|
Регуля-торные |
Регулируют деятельность половых и щитовидной желез и над-почечников |
Усиливают гор-мональную актив-ность всех желез |
Усиливают отделение воды при образовании вторичной мочи (потеря воды) |
|||
|
Щитовид-ная |
Поверх щи-товидного хряща гортани |
Две доли, соединен-ные пере-мычкой и состоящие из пузырь-ков |
С кровью разносится по организ-му, регули-руя обмен веществ. По-вышает воз-будимость нервной системы |
Базедова болезнь, выражающаяся в повышении обме-на веществ, воз-будимости нерв-ной системы, раз-витии зоба |
Микседема, выражающа-яся в понижении обмена веществ, возбудимости нервной системы, отеч-ности. В молодом возрасте – карликовость и крети-низм |
|
|
Надпочеч-ники |
Над верхней частью почек |
Двухслой-ные. На-ружный слой – кор-ковый, внутрен-ний – моз-говой |
Корти-коиды |
Регулируют обмен минеральных и органических веществ, выделение половых гормонов |
Раннее половое созревание с быстрым прекращением роста |
Бронзовая болезнь (бронзовый оттенок кожи, слабость, похудение). Удаление коры надпочечников вызывает смерть вследствие потери большого количества натрия |
|
Адрена-лин |
Ускоряет работу серд-ца, сужает кровеносные сосуды, тор-мозит пище-варение, расщепляет гликоген |
Учащенное серд-цебиение, повы-шение пульса и кровяного давле-ния, особенно при испуге, страхе, гневе |
Количество регулируется нервной системой, поэто-му его недостатка практи-чески не бывает |
|||
|
Поджелудочная железа |
полость тела ниже желуд-ка |
“Остров-ки” клеток, располо-женные в разных местах железы |
Регулирует содержание глюкозы в крови, синтез гликогена из избытка глюкозы |
Шок, сопровож-дающийся судо-рогами и потерей сознания при падении уровня глюкозы в крови |
Сахарный диабет, при котором уровень глюкозы в крови повышается, появляется сахар в моче |
Растения, как и животные, также секретируют свои собственные гормоны. Эти вещества вырабатываются в меристемах, расположенных на корнях и стволе, и оказывают свое влияние через различные каналы, переносящие сок растений.
У здорового человека вырабатывается то количество гормонов, которое требуется его организму, но иногда наблюдаются органические нарушения, приводящие к излишнему образованию гормонов (гиперфункция) или к недостаточному образованию (гипофункция).
Одной из этих аномалий является зоб, вызываемый гиперфункцией щитовидной железы. Эта железа увеличивается в размере и приводит к пучеглазию.
Другая болезнь, связанная с гиперфункцией, - это гигантизм, при котором происходит избыточное производство гипофизарного гормона. Ее симптомы - разрастание лица, кистей рук и стоп.
Акромегалия - это утолщения конечностей, губ, к которым приводит переизбыток гормона роста в организме.
Наиболее известная болезнь, вызванная гипофункцией, - сахарный диабет, появляющийся из-за недостатка инсулина, что приводит к повышению уровня глюкозы в крови.
Среди других отклонений встречается кретинизм (гипофункция щитовидной железы в детстве), болезнь Аддисона (гипофункция коры надпочечников).
Половые железы (рис. 369, 370).
Влияние, которое оказывает на организм удаление половых желез, известно давно, так как кастрация скота применялась еще в древности для повышения рабочих качеств домашнего скота и увеличения его веса. Однако только в середине XIX века было точно установлено, что влияние половых желез на волосяной покров, рост, телосложение и поведение зависит от поступления в кровь особых веществ, вырабатываемых семенниками особей мужского пола и яичниками особей женского пола.

Рисунок 369. Яичко (testis ). Мужская половая железа. 1 – семенной канатик; 2 – фасция мышцы, поднимающей яичко; 3 – внутреняя семенная фасция. 4 – лозовидное венозное сплетение; 5 – влагалишная оболочка яичка (серозная); 6 – головка придатка яичка; 7 – привесок придатка яичка; 8 – привесок яичка; 9 – яичко; 10 – мошонка; 11 – хвост придатка яичка; 12 -семявыносящий проток.

Рисунок 370. Яичник (ovarium ). Женская половая железа. 1 – маточная труба; 2 – надъяичник (придаток яичника); 3 – яичниковая артерия; 4 – бахромка трубы (маточной); 5 -связка, подвешивающая яичник; 6 – артерии и вены яичника; 7 – яичник; 8 – круглая связка матки; 9 – широкая связка матки; 10 – маточные вены; 11 – маточная артерия; 12 – влага-лише; 13 – матка; 14 – собственная связка яичника; 15 – яичниковая ветвь маточной артерии.
Эти вещества - мужской гормон тестостерон и его производное андростерон и женский гормон эстрадиол.
Половые железы выполняют две функции: они вырабатывают половые клетки и половые гормоны. В мужских половых железах - семенниках - образуются сперматозоиды, а в специальных интерстициальных клетках вырабатывается половой гормон - тестостерон. В яичниках образуются яйцеклетки и гормоны. В созревающем фолликуле развивается яйцеклетка и выделяется гормон фолликулин, или эстрадиол. На месте лопнувшего фолликула развивается желтое тело, которое вырабатывает второй гормон - прогестерон. Этот гормон иначе называют гормоном беременности. Мужской половой гормон - тестостерон - стимулирует развитие вторичных половых признаков (рост бороды, характерное распределение волос на теле, развитие мускулатуры и др.) и всего облика, свойственного мужчине.
Андрогены обуславливают развитие полового аппарата и рост половых органов, развитие половых признаков: тембра голоса, строения гортани, скелета, мускулатуры и др. Совместно с ФСГ гипофиза тестостерон активирует сперматогенез. Гиперфункция семенников в раннем возрасте ведет к раннему половому созреванию, быстрому росту тела и развитию вторичных половых признаков. Поражение семенников или кастрация затормаживает или останавливает эти процессы.
Гиперфункция яичников вызывает раннее половое созревание с выраженными вторичными половыми признаками и менструацией. Описаны случаи раннего полового созревания в 4-5 лет!
Количество половых гормонов, обнаруживаемых в крови, очень низкое в первые дни жизни, и постепенно увеличивается, ускоряя темпы развития, особенно в период второго детства (8-12 лет у мальчиков и 8-11 - у девочек), подростковом (13-16 лет мальчики, 12-15 лет девочки) и юношеском (17-21 год юноши и 16-20 лет девушки). В данных возрастных периодах деятельность половых желез имеет важное значение для темпов роста, формо-образования и интенсивности протекания обмена веществ, то есть может выступать в роли ведущего фактора развития. По мере старения организма, чаще всего к 70 годам, наблюдается падение инкреции гонад, имеющее важное значение в процессе общего «увядания» организма.
Как показывают данные исследований, наиболее значительные перестройки организма, и в частности, его эндокринной системы происходят в период полового созревания. В ходе этого периода человек достигает биологической зрелости. Под влиянием гормонов эндокринных желез происходит окончательное формирование половых органов и желез, развиваются вторичные половые признаки, по которым один пол отличается от другого.
Половое созревание у девочек начинается раньше, чем у мальчиков. Начиная с 7-8 лет жировая клетчатка распределяется уже по женскому типу: жир откладывается в молочных железах, на бедрах, отчего формы тела округляются вначале в области бедер и туловища, а затем в области плечевого пояса и рук. В 13-15 лет наблюдается быстрый рост тела в длину, появляется растительность на лобке и в подмышечных впадинах. Характерные изменения происходят и в половых органах: увеличивается в размерах матка, в яичниках созревают фолликулы, начинается менструация. Для девушек 19-20 лет - время окончательного становления менструальной функции и наступления анатомической и физиологической зрелости всего организма.
У мальчиков половое созревание начинается с 10-11 лет, в 12-13 лет меняется форма гортани и ломается голос, в 13-14 лет начинается формирование скелета по мужскому типу. В 15-16 лет усиленно растут волосы под мышками и на лобке, а также появляются на лице. В 24-25 лет заканчивается полное окостенение скелета.
Сложные процессы, протекающие в детском организме в переходном периоде нельзя, конечно, объяснить только изменениями, происходящими в половой сфере. Перестраивается весь организм. Он быстро развивается, усиленно работают внутренние органы, меняется психика.
Период полового созревания сравнительно продолжителен. При этом происходит неравномерное развитие различных функциональных систем, нарушается гармония в деятельности внутренних органов. Сердце опережает в росте кровеносные сосуды, вследствие чего повышается артериальное давление, что снижает в конечном счете эффективность работы самого сердца и нередко приводит к головокружениям. В этом лежит причина головных болей, снижения работоспособности, периодических приступов вялости. Нередко у подростков возникает обморочное состояние из-за спазмов мозговых сосудов. Все эти нарушения, как правило, исчезают с окончанием периода полового созревания.
У подростка рост конечностей опережает рост туловища, в связи с этим движения становятся угловатыми, плохо скоординированными. Вместе с тем возрастает мышечная сила, особенно к концу периода. Рост мышечной массы у мальчиков приводит к потребности упражнять ее. Поэтому очень важно разумно направить эту энергию на нужную работу.
Интенсивный рост, резкое усиление функций желез внутренней секреции, структурные и физиологические перестройки организма повышают возбудимость ЦНС. Эмоции подростков подвижны, изменчивы, противоречивы. Повышенная чувствительность сочетается нередко с черствостью, застенчивость - с развязностью, проявляется чрезмерный критицизм (юношеский максимализм) и нетерпимость к опеке родителей. В этот период иногда наблюдается невротические реакции, раздражимость, у девочек - плаксивость (в период менструации). Возникают новые отношения между полами. У девочек обостряется интерес к своей внешности. Мальчики стараются показать перед девочками свою силу, появляются первые любовные «переживания».
В этот период не стоит привлекать внимание подростков к сложным изменениям в их организме, психике, но объяснять закономерности и биологический смысл этих изменений необходимо. Искусство педагога, воспитателя в этот период заключается в том, чтобы найти такие формы и методы работы, которые бы переключали внимание детей с сексуальных переживаний на разнообразные виды деятельности.
Вилочковая железа , или тимус расположен в верхнем отделе переднего средостения. Закладывается на 6 неделе эмбрионального развития. При рождении масса железы равна 10-15 г, максимального значения она достигает к 11-13 годам (35-40 г). После 13 лет постепенно происходит возрастная эволюция вилочковой железы и к 75 годам ее масса составляет в среднем всего 6 г.
Тимусу принадлежит важная роль в иммунологической защите организма, в частности в образовании иммунокомпетентных клеток. Под влиянием гормона тимозина, стволовые клетки превращаются в Т-лимфоциты, которые затем поступают в лимфатические узлы. У детей с врожденным недоразвитием тимуса возникает лимфопения (снижение количества иммунных тел). С деятельностью железы связан период наиболее интенсивного роста организма. До сих пор не получен гормон вилочковой железы в чистом виде.
Гипофиз (рис. 371, 372) - одна из центральных желез внутренней секреции, расположена под основанием головного мозга в углублении турецкого седла черепа и имеет массу 0,5-0,7 г.

Рисунок 371. Гипофиз (hipophysis ). Положение гипофиза в области основания головного моз-га. Сагиттальный разрез мозга. Вид с медиальной стороны. 1 – мозолистое тело; 2 – свод; 3 -таламус; 4 – третий желудочек; 5 – гипоталамус; 6 – средний мозг; 7 – серый бугор; 8 -глазодвигательный нерв; 9 – воронка; 10 – инфундибулярная часть гипофиза; 11 – гипофиз; 12 -перекрест зрительный нервов; 13 – передняя (белая) спайка.

Рисунок 372. Гипофиз (hipophysis ) и его взаимоотношения с кровеносными сосудами головного мозга и с черепными нервами. Вид снизу. 1 – передняя мозговая артерия; 2 – зритель-ный нерв; 3 – перекрест зрительных нервов; 4 – внутренняя сонная артерия; 5 – средняя мозговая артерия; 6 – воронка (серого бугра); 7 – гипофиз; 8 – задняя мозговая артерия; 9 -глазодвигательный нерв; 10 – основная (базилярная) артерия; 11 – мост (мозга); 12 – артерия лабиринта; 13 – задняя соединительная артерия; 14 – зрительный тракт; 15 – серый бугор; 16 – обонятельный тракт.
Гипофиз состоит из трех долей: передней, средней и задней, окруженных общей капсулой из соединительной ткани. Один из гормонов передней доли оказывает влияние на рост (рис. 373). Избыток этого гормона в молодом возрасте сопровождается резким усилением роста - гигантизм, а при повышенной функции гипофиза у взрослого, когда рост тела прекращается, наступает усиленный рост коротких костей: предплюсны, плюсны, фаланг пальцев, а также мягких тканей (языка, носа). Такая болезнь называется акромегалией. Пониженная функция передней доли гипофиза приводит к карликовому росту. Гипофизарные карлики пропор-ционально сложены и нормально умственно развиты. В передней доле гипофиза образуются также гормоны, влияющие на обмен жиров, белков, углеводов. В задней доле гипофиза вырабатывается антидиуретический гормон, который снижает скорость образования мочи и изменяет водный обмен в организме.

Рисунок 373. Гигантизм и карликовый нанизм.
В передней доле гипофиза, или аденогипофизе, железистые клетки выделяют шесть тропных гормонов, то есть гормонов, стимулирующих другие эндокринные железы.
Тиреотропный гормон , или гормон, стимулирующий щитовидную железу (ТТГ): стимулирует секрецию щитовидной железы.
Гонадотропный , или фолликулостимулирующий гормон (ФСГ): стимулирует развитие фолликула яичника у женщин и созревание сперматозоидов у мужчин.
Лютеинизирующий гормон (ЛГ): стимулирует овуляцию у женщин и выработку тестостерона у мужчин.
Адренокортикотропный гормон (АКТГ): стимулирует кору надпочечников с целью выработки кортикостероидных гормонов.
Пролактин : стимулирует секрецию молока молочными железами.
Гормон роста (СТГ) (соматотропин): стимулирует рост костей и мышц, усиливая митоз и поступление в клетки аминокислот.
Промежуточная доля гипофиза секретирует один-единственный гормон - меланостимулирующий гормон (МСГ), помогающий синтезировать меланин. Задняя доля гипофиза, или нейрогипофиз, выполняет функцию депо гормонов, синтезированных в гипоталамусе.
Гипоталамус, расположенный над гипофизом головного мозга, является центральным органом гормональной системы (рис. 374): он регулирует выделение и распределение гормонов в нужных количествах и в нужное время.
Это место, куда поступают все сигналы, идущие от всех нервных клеток головного мозга.  Затем он на основе этой информации передает необходимые команды в гипофиз.
Затем он на основе этой информации передает необходимые команды в гипофиз.
Кроме своих функций, связанных с нервной системой, гипоталамус выполняет также эндокринную функцию, так как его нервные клетки высвобождают нейрогормоны, вырабатываемые не собственно эндокринной железой. Два из них хранятся в гипофизе: окситоцин, регулирующий сокращения матки во время родов, и вазопрессин, или антидиуретический гормон, регулирующий водный обмен и стимулирующий обратную резорбцию воды в почках и сужающий сосуды.
АКТГ вызывает раздражение пучковой и сетчатой зон надпочечников и усиливает синтез их гормонов. При удалении гипофиза у животного указанные зоны надпочечников подверглись Рисунок 374. атрофии вследствие отсутствия АКТГ. Секреция АКТГ усиливается при воздействии всех чрезвычайных раздражителей, вызывающих стресс, это вызывает усиление выработки глюкокортикоидов (способствующих повышению сопротивляемости организма неблагоприятным факторам).
Интенсивность синтеза АКТГ в гипофизе у детей больше, чем у взрослых, и снижается в дальнейшем с возрастом, что может объяснять снижение барьерной (защитной) функции организма к заболеваниям в стареющем организме.
В передней доле гипофиза продуцируются гормоны, общее название которых гонадо-тропные гормоны (ФСГ, ЛГ). Фолликулостимулирующий гормон стимулирует рост и развитие фолликулов яичников и выход из них эстрогенов, а также рост яичек и сперматогенез.
ЛГ вызывает периодический выход яйцеклетки из яичника (овуляцию), а также развитие после этого желтого тела, способствует росту и развитию яичка, выработке андрогенов.
В первые годы после рождения в гипофизе мальчиков и девочек гонадотропные гормоны почти отсутствуют. С возрастом в гипофизе женщин, и в меньшей степени - мужчин, происходит повышение концентрации гонадотропинов, которое длится и после наступления менопаузы.

Рисунок 375. Возрастные изменения гонадотропинов в моче мужчин и женщин.
Об инкреции гонадотропинов можно судить по выведению их с мочой. На рис. 357 показано, что у детей обеих полов до периода полового созревания сколь либо существенного количества этих гормонов не обнаружено. Женщины до менопаузы выделяют все увеличивающиеся с возрастом количество гормонов, возрастающее в 4 раза в период от 10 до 50 лет. В старческом возрасте величина гонадотропинов продолжает увеличиваться. У мужчин происходит небольшое возрастное увеличение выделения этого гормона с мочой.
Щитовидная железа (рис. 376) расположена в передней области шеи, весит 30-60 г и состоит из двух долей, соединенных перешейком.

Рисунок 376. Щитовидная железа (glandula thyroidca ). Вид спереди. 1 – щито-подъязычная мышца; 2 – пирамидальная доля щитовидной железы; 3 – верхняя щитовидная артерия; 4 -левая доля щитовидной железы; 5 – перешеек щитовидной железы; 6 – нижняя щитовидная вена; 7 – трахея; 8 – нижняя щитовидная артерия; 9 – непарная щитовидная вена; 10 – правая доля щитовидной железы; 11 – верхняя щитовидная вена; 12 – щитовидный хрящ; 13 – верхняя гортанная артерия; 14 – подъязычная кость.
Щитовидная железа вырабатывает и секретирует в кровь тиреоидные гормоны - тироксин и трийодтиронин, оказывающие мощное регулирующее влияние на основные функции организма - его рост, развитие и обмен веществ (ускоряет катаболические процессы, что ведет к повышению температуры, высокому расходу питательных веществ). Недостаточная функция щитовидной железы в детском возрасте приводит, как известно, к развитию кретинизма (задержке роста, нарушению пропорций тела при задержке полового и умственного развития). У взрослых гипофункция вызывает развитие микседемы (снижение основного обмена на 30-40%, что ведет к увеличению веса тела за счет жира, отекам).
Гиперфункция в данном случае приводит к Базедовой болезни, или тиреотоксикозу. Болезнь сопровождается сильным похудением, пучеглазостью.
В первые недели после рождения инкреция железы еще низка, но затем она возрастает к периоду половой зрелости и в последующем онтогенезе меняется мало, несколько снижаясь к старости. Гистологические изменения в пожилом и старческом возрасте заключаются в понижении диаметра фолликулов, атрофии секреторного эпителия. В старости же в большинстве случаев понижается поглощение радиоактивного йода. С возрастом изменяется не только количество выработанного гормона, но и восприимчивость тканей к его действию.
В первые месяцы жизни опытные животные и человек слабо реагируют на введение тироксина. С этой низкой реактивностью тканей молодых животных совпадает еще недостаточная активность самой железы. По-видимому, в раннем возрасте высокий собственный метаболизм не нуждается во «взвинчивании» его гормонами. К старости организм, хотя и сохраняет большую чувствительность к гормону, уже не способен поднять уровень своих окислительных процессов.
Внутри железы имеются небольшие полости, или фолликулы, наполненные слизистым веществом, содержащим гормон тироксин. В состав гормона входит йод. Этот гормон влияет на обмен веществ, особенно жиров, на рост и развитие организма, усиливает возбудимость нервной системы, деятельность сердца. При разрастании ткани щитовидной железы количество гормона, поступающего в кровь, увеличивается, что приводит к заболеванию, которое называется базедовой болезнью. У больного повышается обмен веществ, что выражается в сильном исхудании, повышенной возбудимости нервной системы, усиленном потоотделении, быстрой утомляемости, пучеглазии.
При пониженной функции щитовидной железы возникает заболевание микседема, проявляющееся в слизистом отеке тканей, замедлении обмена веществ, задержке роста и развития, ухудшении памяти, нарушении психической деятельности. Если это случается в раннем детском возрасте, развивается кретинизм (слабоумие), характеризующийся умственной отсталостью, недоразвитием половых органов, карликовым ростом, непропорциональным строением тела. В горных районах встречается заболевание, известное под названием эндемический зоб, возникающее вследствие недостатка йода в питьевой воде. При этом ткань железы, разрастаясь, на некоторое время возмещает дефицит гормона, но и в этом случае его может быть недостаточно для организма. В целях профилактики эндемического зоба жителям соответствующих зон поставляют обогащенную йодом поваренную соль или добавляют ее в воду.
Околощитовидные железы (рис. 377) - четыре небольших тельца, расположенные позади боковых долей щитовидной железы, в ее капсуле, по два с каждой стороны. Таким образом, различают верхние и нижние околощитовидные железы. К концу внутриутробного развития около-щитовидные железы являются вполне сформированными анатомическими образованиями, окруженными соединительно-тканной капсулой. После рождения их масса нарастает: у мужчин - до 30 лет, а у женщин - до 40-50 лет. В процессе старения ткань околощитовидных желез частично замещается жировой и соединительной.
Паратгормон относится к гормонам пептидной природы. Он регулирует уровень кальция в крови, способствуя распаду костной ткани и выведению в кровь кальция.
Функция желез активируется на 3-4 неделе постнатальной жизни, достигая максимума в 6-10 лет, при этом наряду с прогрессивным изменением тканей встречаются и признаки регресса (появление оксифильных клеток и накопление коллоида). К 50 годам отмечается вытеснение паренхимы железы жировой тканью. Падает с возрастом и способность клеток активировать паратгормон. При гипофункции паращитовидных желез возникает заболевание тетания, характерным симптомом которой являются приступы судорог. В крови снижается содержание кальция, что ведет к размягчению костей. При избытке кальция в крови он откладывается в необычных для него местах - в сосудах, аорте, почках.

Рисунок 377. Паращитовидные (околощитовидные) железы (giandulae parathyroidei ). Вид сзади. 1 – средний констриктор (сжиматель) глотки; 2 – нижний констриктор глотки; 3 -правая верхняя околощитовидная железа; 4 – правая доля щитовидной железы; 5 – правая нижняя околощитовидная железа; 6 – трахея; 7 – пищевод; 8 – левая нижняя околощитовид-ная железа; 9 – левая доля щитовидной железы; 10 – левая верхняя околощитовидная железа.
Обобщая результаты, полученные современной возрастной физиологией и биохимией, следует прежде всего отметить, что несмотря на значительный экспериментальный материал, пока еще нет возможности создать целостную картину возрастного развития эндокринной системы.
В онтогенезе эндокринной регуляции могут изменяться в зависимости от четырех основных переменных:
1) С возрастом может изменяться уровень и качество инкреции самих желез, как следствие их собственного старения.
2) С возрастом могут измениться коррелятивные соотношения между отдельными железами (иная «эндокринная формула»).
3) Может изменяться нервная регуляция эндокринных желез.
4) Изменяется восприимчивость тканей, их чувствительность и реактивность.
Надпочечники (рис. 378) - парные железы, расположенные у верхнего края почек. Их масса - около 12 г каждая, вместе с почками они покрыты жировой капсулой. В них различают корковое, более светлое вещество, и мозговое, темное. Надпочечники - парный орган в виде телец, расположенный над почками. Масса каждого из них составляет 8-10 г. Надпочечники состоят из двух совершенно самостоятельных частей: темного мозгового вещества, лежащего внутри, и бледного наружного слоя - коры. Из коркового вещества надпочечников в настоящее время выделено 50 стероидных соединений. Обнаружено 8 биологически активных кортикостероидов, однако истинными гормонами являются кортизол (гидрокортизон), кортикостерон, альдостерон и др. В паренхиматозных клетках мозгового вещества надпочечников образуются адреналин и норадреналин.
В корковом слое надпочечников вырабатываются кортикостероиды или кортикоиды. Их 3 группы:
1) глюкокортикоиды - гормоны, действующие на обмен веществ, особенно на обмен углеводов. Сюда относятся гидрокортизон, кортизол и кортикостерон. Отмечена высокая способность глюкокортикоидов подавлять образование иммунных тел, что позволило использовать эти гормоны при трансплантации органов (сердца, почек и др.) с целью снижения неблагоприятного иммунного ответа.
2) минералокортикоиды, регулирующие минеральный и водный обмен.
3) андрогены и эстрогены - аналоги мужских и женских половых гормонов. Эти гормоны менее активны, чем гормоны половых желез и вырабатываются в небольших количествах.

Рисунок 378. Надпочечная железа (надпочечник, левый) (glandula suprarenalis ). Вид спереди. 1 – надпочечник; 2 – нижняя надпочечниковая вена; 3 – нижняя надпочечниковая артерия; 4 -почечная артерия (левая); 5 – почка (левая); 6 – левая яичковая вена; 7 – мочеточник; 8 – верхняя брыжеечная артерия; 9 – почечная вена (левая); 10 – яичковая артерия; 11 – правая яичковая вена; 12 – нижняя полая вена; 13 – чревный ствол; 14 – аорта; 15 – средняя надпочечниковая артерия; 16 – нижняя диафрагмальная артерия (левая); 17 – верхние надпочечниковые артерии.
Мозговая часть надпочечников вырабатывает гормоны адреналин и норадреналин. Эти гормоны - важная часть адаптационно-трофической системы, образованной гипоталамо-гипофизарно-надпочечниковым комплексом, и наиболее известны нам как стрессорные гормоны.
Инкреция кортикостероидов корковым слоем надпочечников возникает в эмбриогенезе сравнительно рано - на 7-8 неделе внутриутробного развития. Общий уровень выработке кортикостероидов нарастает сначала медленно, а затем быстро, достигая максимума в 20 лет, а затем падает к старости. При этом быстрее всего к старости уменьшается выработка минералокортикоидов, несколько медленнее - андростероидов и еще медленнее - глюкокортикоидов.
Адреналин и норадреналин появляются в мозговом веществе надпочечников очень рано. Уже при рождении уровень инкреции адреналина в надпочечниках сопоставим с уровнем взрослого человека. (Выделение катехоламинов в моче у молодых, зрелых и пожилых людей почти не изменяется с возрастом).
В корковом слое вырабатываются несколько гормонов - кортикостероидов, оказывающих влияние на солевой и углеводный обмены, способствующих отложению гликогена в клетках печени и поддерживающих постоянную концентрацию глюкозы в крови. При недостаточной функции коркового слоя развивается Аддисонова болезнь, сопровождающаяся мышечной слабостью, одышкой, потерей аппетита, уменьшением концентрации в крови сахара, понижением температуры тела. Кожа при этом приобретает бронзовый оттенок - характерный признак данного заболевания. В мозговом слое надпочечников вырабатывается гормон адреналин. Его действие многообразно: он увеличивает частоту и силу сердечных сокращений, повышает кровяное давление (при этом просвет многих мелких артерий сужается, а артерии головного мозга, сердца и почечных клубочков расширяются), усиливает обмен веществ, особенно углеводов, ускоряет превращение гликогена (печени и работающих мышц) в глюкозу, в результате чего работоспособность мышц восстанавливается.
Поджелудочная железа (рис. 379) располагается позади желудка, обычно на уровне первого и второго поясничных позвонков, и занимает пространство от двенадцатиперстной кишки до ворот селезенки.

Рисунок 379. Поджелудочная железа (pancreas ). Панкреатические островки. 1 – тело поджелудочной железы; 2 – селезеночная артерия; 3 – селезеночная вена; 4 – хвост поджелу-дочной железы; 5 – верхняя брыжеечная артерия; 6 – верхняя брыжеечная вена; 7 – восходящая часть двенадцатиперстной кишки; 8 – нижняя брыжеечная артерия; 9 – аорта; 10 – крючко-видный отросток поджелудочной железы; 11 – нижняя (горизонтальная) часть двенадцати-перстной кишки; 12 – нижняя поджелудочно-двенадцатиперстная артерия; 13 – головка поджелудочной железы; 14 – нисходящая часть двенадцатиперстной кишки; 15 – верхняя (горизонтальная) часть двенадцатиперстной кишки; 16 – верхняя поджелудочно-двенадцати-перстная артерия; 17 – пилорический отдел желудка (отрезан); 18 – нижняя полая вена; 19 -аорта.
Длина ее - 10-23 см, ширина - 3-9 см, толщина - 2-3 см, масса - 70-100 г. В поджелудочной железе различают три отдела: головку, тело и хвост. Она функционирует как смешанная железа, гормон которой - инсулин
- вырабатывается клетками островков Лангерганса. Эндокринную функцию поджелудочной железы осуществляют клетки, расположенные в виде островков (рис. 380) (островки Лангерганса). Эти клетки вырабатывают гормон -  инсулин. Инсулин действует главным образом на углеводный обмен, оказывая действие, противоположное адреналину. Основная функция инсулина - сохранение углеводов в организме и пополнение запасов глюкагона. При снижении выработки инсулина большая часть глюкозы выводится из организма с мочой (диабет). Гормоны вырабатываются в поджелудочной железе клетками островков Лангерганса. Альфа-клетки вырабатывают гормон глюкагон, который способствует превращению гликогена печени в глюкозу крови, в результа- Рисунок
380. те чего увеличивается количество сахара в крови. Второй гормон - инсу-лин - вырабатывается бета-клетками островков поджелудочной железы. Он способствует отложению гликогена в печени и уменьшению количества сахара в крови. При недостаточной функции поджелудочной железы, появляющейся в результате ее заболевания или частичного удаления, развивается тяжелое заболевание - сахарный диабет.
инсулин. Инсулин действует главным образом на углеводный обмен, оказывая действие, противоположное адреналину. Основная функция инсулина - сохранение углеводов в организме и пополнение запасов глюкагона. При снижении выработки инсулина большая часть глюкозы выводится из организма с мочой (диабет). Гормоны вырабатываются в поджелудочной железе клетками островков Лангерганса. Альфа-клетки вырабатывают гормон глюкагон, который способствует превращению гликогена печени в глюкозу крови, в результа- Рисунок
380. те чего увеличивается количество сахара в крови. Второй гормон - инсу-лин - вырабатывается бета-клетками островков поджелудочной железы. Он способствует отложению гликогена в печени и уменьшению количества сахара в крови. При недостаточной функции поджелудочной железы, появляющейся в результате ее заболевания или частичного удаления, развивается тяжелое заболевание - сахарный диабет.
Инсулиновый аппарат поджелудочной железы развивается очень рано. С возрастом увеличивается общее количество островков Лангерганса, но при пересчете на единицу массы их количество, наоборот, значительно снижается по мере старения. Было также отмечено и возрастное уменьшение гормона в эндокринной железе.
На рис.381 показан средний уровень содержания в крови инсулина и глюкозы. Как видно из таблиц, содержание инсулина с возрастом несколько повышается, но недостаточно для снижения уровня сахара в крови, что говорит о подавлении инсулиновой функции в позднем онтогенезе. Это подтверждается и в опытах на животных.

Рисунок 381. Средний уровень содержания в крови инсулина и глюкозы у человека.
В пользу некоторой инсулиновой недостаточности в старости свидетельствуют и данные исследований при одинарной и двойной сахарной нагрузке и установивших высокую толерантность молодых и зрелых индивидуумов (в пределах от 5 до 50-летнего возраста).
Так, на рис. 382 показана выраженность гипергликемии и скорость ее устранения при двойной глюкозной нагрузке у людей разного возраста.

Рисунок 382. Выраженность гипергликемии и скорость ее устранения при двойной глюкозной нагрузке у людей разного возраста.
Особенно ярко заметна удивительная высокая толерантность к сахарным нагрузкам детей и юношей, которая несколько снижается в зрелом возрасте и очень существенно снижена в старости. Поэтому является обоснованным считать употребление больших количеств сахара в молодости и необходимо ограничение его потребления в старости, так как нарастает угроза возникновения диабета.
Инсулин регулирует углеводный обмен, т.е. способствует усвоению клетками глюкозы, поддерживает ее постоянство в крови, переводя глюкозу в гликоген, который откладывается в печени и мышцах. Второй гормон этой железы - глюкагон. Его действие противоположно инсулину: при недостатке глюкозы в крови глюкагон способствует превращению гликогена в глюкозу. При пониженной функции островков Лангерганса нарушается обмен углеводов, а затем белков и жиров. Содержание глюкозы в крови возрастает с 0,1 до 0,4%, она появляется в моче, а количество мочи увеличивается до 8-10 л. Это заболевание называется сахарным диабетом. Его лечат путем введения человеку инсулина, извлеченного из органов животных.
Деятельность всех желез внутренней секреции взаимосвязана: гормоны передней доли гипофиза способствуют развитию коркового вещества надпочечников, усиливают секрецию инсулина, влияют на поступление в кровь тироксина и на функцию половых желез. Работу всех желез внутренней секреции регулирует центральная нервная система, в которой находится ряд центров, связанных с функцией желез. В свою очередь гормоны влияют на деятельность нервной системы. Нарушение взаимодействия этих двух систем сопровождается серьезными расстройствами функций органов и организма в целом.
Эпифиз, или шишковидное тело (рис. 383) - овальное железистое образование, относящееся к промежуточному мозгу.

Рисунок 383. Эпифиз (epiphysis ). Вид сверху. 1 – внутренние мозговые вены; 2 – третий желудочек; 3 – эпифиз; 4 – большая вена мозга; 5 – сосудистое сплетение бокового желудочка; 6 – таламус; 7 – столбы свода мозга.
Эпифиз расположен между зрительными буграми и четверохолмием. Длина его - 8 мм, вес, в среднем, - 0,118 г, ширина - 4-6 мм. Паренхиму эпифиза составляют крупные светлые клетки, состоящие из цитоплазмы и ядер с базофильной зернистостью и содержащие нуклеиновые кислоты РНК и ДНК. Инволюция эпифиза начинается с 4-5-летнего возраста. После 8 лет в эпифизе происходит обызвествление, состоящего из органической основы, карбоната и фосфата кальция и магния. Эпифиз считают железой внутренней секреции, однако роль его в организме еще полностью не изучена. Он участвует в регуляции обмена фосфора, калия, кальция и магния, а также водно-солевого обмена. Основным гормоном эпифиза является мелатонин - ингибитор развития и функционирования половых желез. Обнаружено, что поражение эпифиза у детей сопровождается преждевременным половым созреванием, то есть ему принадлежит сдерживающее влияние на развитие половых желез.
Таким образом, эпифиз раннего детства может выполнять свою сдерживающую функцию, продуцируя повышенное количество мелатонина. Максимальная активность в раннем детстве (5-7 лет) и именно к этому периоду относится максимальное сдерживающее влияние. Позднее эпифиз подвергается значительной инволюции, правда весьма неравномерной.
В слизистой оболочке желудка и кишечника
(рис. 384) имеются не собственно железы, а разрозненные  клетки эндокринного типа. Выделяемые ими желудочно-кишечные гормоны регулируют пищева-рительные процессы, активизируя выделение различных соков или вызывая угнетающий эффект.
клетки эндокринного типа. Выделяемые ими желудочно-кишечные гормоны регулируют пищева-рительные процессы, активизируя выделение различных соков или вызывая угнетающий эффект.
Гастрин стимулирует слизистую оболочку желудка, когда в нее попадает пищевой комок.
Его антагонист энтерогастрон, вырабатываемый в слизистой оболочке двенадцатиперстной кишки, сокра-щает выделение соков и частоту перистальтических дви-жений.
В двенадцатиперстной кишке вырабатываются панкреозимин и секретин, стимулирующие выделение поджелудочного сока, а также холецистокинин, способст-вующий выбросу желчи при поступлении жирных веществ.
И, наконец, энтерокинин, вырабатываемый в слизис-той оболочке кишечника, стимулирует выделение сока в этом органе.
Рисунок 384.